题目内容
在一定条件下,CO和CH4燃烧的热化学方程式分别为:
2CO(g) + O2(g) = 2CO2(g);△H =-566 kJ/mol
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l);△H =-890 kJ/mol
由1molCO和3molCH4组成的混和气在上述条件下完全燃烧时,释放的热量为
- A.2912kJ
- B.2953kJ
- C.3236kJ
- D.3867kJ
B
试题分析:根据反应的热化学方程式可知,1molCO和3molCH4组成的混和气在上述条件下完全燃烧时,释放的热量为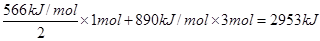 ,答案选B。
,答案选B。
考点:考查反应热的计算
点评:该题是高考中的常见题型,属于基础性试题的考查。试题基础性强,侧重对学生反应热含义和计算熟悉掌握程度,有利于提高学生的应试能力和学习效率。
试题分析:根据反应的热化学方程式可知,1molCO和3molCH4组成的混和气在上述条件下完全燃烧时,释放的热量为
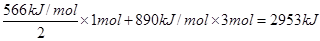 ,答案选B。
,答案选B。考点:考查反应热的计算
点评:该题是高考中的常见题型,属于基础性试题的考查。试题基础性强,侧重对学生反应热含义和计算熟悉掌握程度,有利于提高学生的应试能力和学习效率。

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
 CO(g)+H2(g)−131.4 kJ。
CO(g)+H2(g)−131.4 kJ。
