题目内容
某同学对H2还原CuO的实验进行了验证.他称取16.0 g CuO,按合理的实验步骤进行实验,至黑色CuO完全变为红色停止加热,继续通H2至试管冷却,称量所得固体产物,质量是13.4 g.
请完成下列问题:
(1)实验所得红色物质的成分是________(写化学式).
(2)已知铜的氧化物都是碱性氧化物.又知Cu+不能稳定存在,在酸性条件下发生歧化反应:2Cu+![]() Cu+Cu2+
Cu+Cu2+
该同学将实验所得物质放入了过量稀H2SO4中,发现溶液为浅蓝色,是何原因?________(写化学反应方程式).
答案:
解析:
解析:
答案:(1)Cu、Cu2O
(2)Cu2O+H2SO4![]() Cu+CuSO4+H2O
Cu+CuSO4+H2O
(或Cu2O+H2SO4![]() Cu2SO4+H2O,Cu2SO4
Cu2SO4+H2O,Cu2SO4![]() Cu+CuSO4)
Cu+CuSO4)
思路解析:(1)如果CuO完全被还原为Cu,则
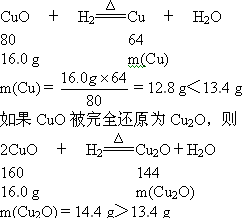
可见CuO的还原产物是Cu和Cu2O.
(2)由题意,Cu2O是碱性氧化物,能跟酸发生复分解反应生成盐和水,即
Cu2O+H2SO4![]() Cu2SO4+H2O
Cu2SO4+H2O
Cu2SO4完全电离,电离出的Cu+在酸性条件下发生歧化反应.即
2Cu+![]() Cu+Cu2+或Cu2SO4
Cu+Cu2+或Cu2SO4![]() Cu+CuSO4
Cu+CuSO4
将以上反应方程式叠加可得总反应方程式.

练习册系列答案
相关题目