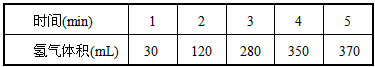题目内容
(1)已知锌与稀硫酸反应为放热反应,某学生为了探究其反应过程中的速率变化,用排水集气法收集反应放出的氢气,实验记录如下
1反应速率最大的(即0~1、l~2、2~3、3~4、4~5min)时间段为
②反应速率最小的时间段为
(2)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,他就分别采取下列措施以减慢反应速率
A.事先在硫酸溶液中加入等体积的蒸馏水
B.将锌粒换成等质量的锌粉
C.事先在硫酸溶液中加入等体积的NaCl溶液
你认为他的做法可行的是
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 30 | 120 | 280 | 350 | 370 |
2~3min
2~3min
.原因是因该反应是放热反应,此时温度高
因该反应是放热反应,此时温度高
②反应速率最小的时间段为
4~5min
4~5min
,原因是因为此时H+浓度小
因为此时H+浓度小
(2)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,他就分别采取下列措施以减慢反应速率
A.事先在硫酸溶液中加入等体积的蒸馏水
B.将锌粒换成等质量的锌粉
C.事先在硫酸溶液中加入等体积的NaCl溶液
你认为他的做法可行的是
A、C
A、C
(填相应字母);做法不可行的理由是将锌粒换成等质量的锌粉,增大了反应的接触面积,化学反应速率加快
将锌粒换成等质量的锌粉,增大了反应的接触面积,化学反应速率加快
.分析:(1)①温度越高,反应速率越快;
②离子浓度越小,反应速率越慢;
(2)增大固体接触面积,反应速率加快,硫酸溶液中加入等体积的NaCl溶液,相当于加水将硫酸稀释,所以氢离子浓度减小.
②离子浓度越小,反应速率越慢;
(2)增大固体接触面积,反应速率加快,硫酸溶液中加入等体积的NaCl溶液,相当于加水将硫酸稀释,所以氢离子浓度减小.
解答:解:(1)①0~1、l~2、2~3、3~4、4~5min各时间段生成氢气的体积分别为30、90、160、70、20,可以看出反应速率最大的是2~3min,锌与稀硫酸反应为放热反应,随反应的进行,温度越来越高,反应速率加快,故答案为:2~3min;因该反应是放热反应,此时温度高;
②随着反应的进行,离子浓度越来越小,反应速率越来越慢,故答案为:4~5min;
(2)A、在硫酸溶液中加入等体积的蒸馏水,相当于加水将硫酸稀释,所以氢离子浓度减小,反应速率减慢,故A正确;
B、将锌粒换成等质量的锌粉,增大固体接触面积,反应速率加快,故B错误;
C、事先在硫酸溶液中加入等体积的NaCl溶液,相当于加水将硫酸稀释,所以氢离子浓度减小,反应速率减慢,故C正确.
故选AC,将锌粒换成等质量的锌粉,增大了反应的接触面积,化学反应速率加快.
②随着反应的进行,离子浓度越来越小,反应速率越来越慢,故答案为:4~5min;
(2)A、在硫酸溶液中加入等体积的蒸馏水,相当于加水将硫酸稀释,所以氢离子浓度减小,反应速率减慢,故A正确;
B、将锌粒换成等质量的锌粉,增大固体接触面积,反应速率加快,故B错误;
C、事先在硫酸溶液中加入等体积的NaCl溶液,相当于加水将硫酸稀释,所以氢离子浓度减小,反应速率减慢,故C正确.
故选AC,将锌粒换成等质量的锌粉,增大了反应的接触面积,化学反应速率加快.
点评:本题考查学生影响化学反应速率的因素,难度不大,但是得分不容易.

练习册系列答案
相关题目
(1)已知锌与稀硫酸反应为放热反应,某学生为了探究其反应过程中的速率变化,用排水集气法收集反应放出的氢气,实验记录如下:
①反应速率最大的(即0min~1min、1min~2min、2min~3min、3min~4min、4min~5min)时间段为______,原因是______
②反应速率最小的时间段为______,原因是:______
(2)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,他就事先在硫酸溶液中分别加入以下物质用以减缓反应速率
A.蒸馏水 B.更加细小的锌粒 C.NaCl溶液
你认为他的做法可行的是______(填相应字母);做法不可行的理由是:______.
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 30 | 120 | 280 | 350 | 370 |
②反应速率最小的时间段为______,原因是:______
(2)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,他就事先在硫酸溶液中分别加入以下物质用以减缓反应速率
A.蒸馏水 B.更加细小的锌粒 C.NaCl溶液
你认为他的做法可行的是______(填相应字母);做法不可行的理由是:______.