题目内容
取等物质的量的MgO和Fe2O3的混合物进行铝热反应,反应的化学方程式为 ,引发铝热反应的实验操作是 。进行铝热反应时,内层纸漏斗底部剪一小孔用水润湿的目的是 。
2Al+Fe2O3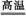 Al2O3+2Fe(2分)
Al2O3+2Fe(2分)
加少量KClO3,插上镁条并将其点燃(2分)
使熔融物易于落下且防止纸漏斗着火(2分)
解析

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
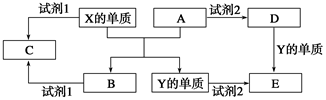
下面是有关物质的转化关系图(有些物质已省略)。
若A为单质,E在常温下为液体,C的相对分子质量为78。请回答下列问题: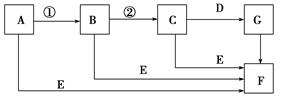
(1)画出A的原子结构示意图________,F的电子式是________。
(2)下面对C物质结构、性质的推断中,不正确的是________。
| A.久置于空气中会变成白色 |
| B.具有强氧化性 |
| C.晶体中存在离子键和共价键 |
| D.遇湿润的紫色石蕊试纸只能使其变蓝色 |