题目内容
16.58.5g NaCl配成500mL溶液,其物质的量浓度为2mol•L-1.分析 根据质量计算NaCl的物质的量,结合c=$\frac{n}{V}$计算浓度.
解答 解:n(NaCl)=$\frac{58.5g}{58.5g/mol}$=1mol,
c(NaCl)=$\frac{1mol}{0.5L}$=2mol/L,
故答案为:2.
点评 本题考查物质的量浓度的计算,为高频考点,侧重于学生的计算能力的考查,注意把握相关计算公式的运用,难度不大.

练习册系列答案
相关题目
6. 人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.如图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )
人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.如图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )
 人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.如图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )
人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.如图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )| A. | 催化剂a表面发生氧化反应,有O2产生 | |
| B. | 催化剂b表面的反应是CO2+2H++2e-═HCOOH | |
| C. | 催化剂a附近酸性减弱,催化剂b附近酸性增强 | |
| D. | 总的电池反应为2H2O+2CO2═2HCOOH+O2 |
11.有(NH4)2SO4和NH4NO3的混合溶液aL,将它均分成两份,一份滴加KOH溶液,刚好使铵离子全部变为NH3;另一份滴加BaCl2溶液,使SO42-离子完全沉淀,反应中消耗x mol KOH,y molBaCl2,据此得知原混合溶液中的c(NO3-)为( )mol•L-1.
| A. | $\frac{2x-4y}{a}$ | B. | $\frac{2x-y}{a}$ | C. | $\frac{x-2y}{a}$ | D. | $\frac{x-2y}{2a}$ |
10.稀土元素是周期表中第ⅢB族钪、钇和镧系元素的总称,它们都是很活泼的金属,性质极为相似,常见化合价为+3.其中钇(Y)元素是激光和超导的重要材料.我国蕴藏着丰富的钇石矿(Y2FeBe2Si2O10),以此矿石为原料生产氧化钇(Y2O3)的主要流程如下:

已知:①有关金属离子形成氢氧化物沉淀时的pH如下表:
②在元素周期表中,铍和铝位于第二周期和第三周期的对角线位置,化学性质相似.
(1)钇石矿(Y2FeBe2Si2O10)的组成用氧化物的形式表示为Y2O3•FeO•2BeO•2SiO2
(2)欲从Na2SiO3和Na2BeO2的混合液中制得Be(OH)2沉淀.则
①最好选用盐酸、b(填字母)两种试剂,再经过必要的操作即可实现.
a.NaOH溶液 b.氨水 c.CO2气体 d.HNO3
②写出Na2BeO2与足量盐酸发生反应的离子方程式:BeO22-+4H+=Be2++2H2O
(3)上述过程中用氨水调节pH=a的目的是使Fe3+完全水解形成沉淀而除去,a应控制在3.7~6.0范围内;写出生成沉淀物A的离子方程式Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+,检验该过程是否沉淀完全的操作方法是取少量滤液,滴加几滴KSCN溶液,观察溶液是否变为血红色,若不变血红色,则说明Fe3+完全沉淀,反之则未完全沉淀.
(4)写出由草酸钇沉淀制备氧化钇的化学方程式Y2(C2O4)3$\frac{\underline{\;高温\;}}{\;}$Y2O3+3CO↑+3CO2↑.

已知:①有关金属离子形成氢氧化物沉淀时的pH如下表:
| 开始沉淀时的pH | 完全沉淀时的pH | |
| Fe3+ | 2.7 | 3.7 |
| Y3+ | 6.0 | 8.2 |
(1)钇石矿(Y2FeBe2Si2O10)的组成用氧化物的形式表示为Y2O3•FeO•2BeO•2SiO2
(2)欲从Na2SiO3和Na2BeO2的混合液中制得Be(OH)2沉淀.则
①最好选用盐酸、b(填字母)两种试剂,再经过必要的操作即可实现.
a.NaOH溶液 b.氨水 c.CO2气体 d.HNO3
②写出Na2BeO2与足量盐酸发生反应的离子方程式:BeO22-+4H+=Be2++2H2O
(3)上述过程中用氨水调节pH=a的目的是使Fe3+完全水解形成沉淀而除去,a应控制在3.7~6.0范围内;写出生成沉淀物A的离子方程式Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+,检验该过程是否沉淀完全的操作方法是取少量滤液,滴加几滴KSCN溶液,观察溶液是否变为血红色,若不变血红色,则说明Fe3+完全沉淀,反之则未完全沉淀.
(4)写出由草酸钇沉淀制备氧化钇的化学方程式Y2(C2O4)3$\frac{\underline{\;高温\;}}{\;}$Y2O3+3CO↑+3CO2↑.
11.某同学用图中四种装置从海带里提取取碘,其中正确且能达到实验目的是( )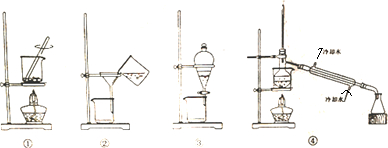

| A. | 装置①将海带灼烧成灰 | B. | 装置②过滤含I-的溶液 | ||
| C. | 装置③放出碘的CCl4溶液 | D. | 装置④分离碘并回收CCl4 |