题目内容
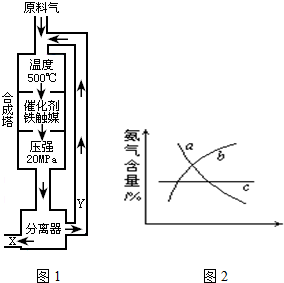
合成氨工厂常通过测定反应前后混合气体的密度来确定氮气的转化率.某工厂测得合成塔中N2,H2混合气体的密度为0.5536g/L(标准状况),从合成塔中出来的混合气体在相同条件下密度为0.693g/L.求该合成氨厂氮气的转化率.
答案:
解析:
解析:
|
解:设N2,H2起始时总物质的量为1mol,N2为x mol,H2为(1-x)mol,根据条件合成塔中N2,H2混合气体的密度在标准状况下为0.5536g/L,用摩尔质量列式可得 28x+2(1-x)=0.5536×22.4 解得x=0.4mol,故H2为0.6mol. 又设0.4mol N2有ymol发生反应, N2+3H2 初始物质的量(mol)0.4 0.6 0 转化物质的量(mol) y 3y 2y 平衡物质的量(mol) 0.4-y 0.6-3y 2y n(总)=0.4-y+0.6-3y+2y=1-2y 根据质量守恒,可得反应式:1×22.4×0.5536=(1-2y)×22.4×0.693 解得y=0.1mol 所以N2转化率为0.1mol/0.4mol×100%=25% |

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
 2NH3
2NH3