题目内容
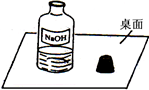 (2013?天河区一模)一天,小明走进实验室,看到了一幅“不和谐”的画面(如图).围绕此瓶试剂是否变质的问题,展开了探究.
(2013?天河区一模)一天,小明走进实验室,看到了一幅“不和谐”的画面(如图).围绕此瓶试剂是否变质的问题,展开了探究.(1)小明提出下列猜想:
猜想一:如果试剂完全变质,则溶液中溶质是
Na2CO3(或碳酸钠)
Na2CO3(或碳酸钠)
;猜想二:如果试剂部分变质,则溶液中溶质是NaOH和Na2CO3;
猜想三:如果试剂没有变质,则溶液中溶质是NaOH.
(2)写出NaOH发生变质的化学反应方程式:
2NaOH+CO2═Na2CO3+H2O
2NaOH+CO2═Na2CO3+H2O
.(3)请你设计实验证实该试剂已经部分变质,完成探究方案:
| 实验步骤 | 预期现象及结论 |
分析:(1)观察图,氢氧化钠溶液敞口放置时能与空气中二氧化碳直接接触,氢氧化钠溶液吸收二氧化碳生成碳酸钠和水而变质;
若全部变质为碳酸钠;若部分变质溶液中溶质是NaOH和Na2CO3;若没变质说明是氢氧化钠;
(2)NaOH发生变质的反应是吸收二氧化碳生成碳酸钠;
(3)如果试剂部分变质,则溶液中溶质是NaOH和Na2CO3;依据碳酸根离子检验方法和碱溶液的检验方法设计实验验证;
若全部变质为碳酸钠;若部分变质溶液中溶质是NaOH和Na2CO3;若没变质说明是氢氧化钠;
(2)NaOH发生变质的反应是吸收二氧化碳生成碳酸钠;
(3)如果试剂部分变质,则溶液中溶质是NaOH和Na2CO3;依据碳酸根离子检验方法和碱溶液的检验方法设计实验验证;
解答:解:(1)观察图,氢氧化钠溶液敞口放置时能与空气中二氧化碳直接接触,氢氧化钠溶液吸收二氧化碳生成碳酸钠和水而变质;全部变质,溶液中溶质为:Na2CO3(或碳酸钠);
故答案为:Na2CO3(或碳酸钠);
(2)图中盛放氢氧化钠溶液的试剂瓶敞口放置,氢氧化钠吸收空气中的二氧化碳生成碳酸钠而变质;
故答案为:CO2+2NaOH=Na2CO3+H2O;
(3)试剂部分变质需要检验溶液中含有碳酸钠和氢氧化钠; 取试剂少许加入足量氯化钡生成白色沉淀证明含有碳酸钠,静止后向上层溶液中滴加酚酞试液,溶液变红证明含有氢氧化钠;
故答案为:
故答案为:Na2CO3(或碳酸钠);
(2)图中盛放氢氧化钠溶液的试剂瓶敞口放置,氢氧化钠吸收空气中的二氧化碳生成碳酸钠而变质;
故答案为:CO2+2NaOH=Na2CO3+H2O;
(3)试剂部分变质需要检验溶液中含有碳酸钠和氢氧化钠; 取试剂少许加入足量氯化钡生成白色沉淀证明含有碳酸钠,静止后向上层溶液中滴加酚酞试液,溶液变红证明含有氢氧化钠;
故答案为:
| 实验操作 | 实验现象及结论 |
| 取少量待测液于试管,加入足量BaCl2溶液 | 产生白色沉淀,则说明溶液中含有Na2CO3 |
| 向静置后的上述试管中,滴加少量酚酞溶液 | 溶液变红(1分),则说明溶液中含有NaOH |
点评:本题考查了实验设计方法,物质验证的反应现象,离子检验的试剂选择,氢氧化钠溶液变质的实质和遍之后物质的判断是解题关键,题目难度中等.

练习册系列答案
相关题目