题目内容
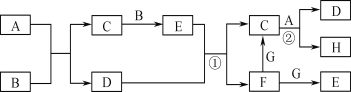
【题目】A,B,C,D四种物质之间的转化关系如图所示![]() 部分产物已略去
部分产物已略去![]() ,下列说法正确的是
,下列说法正确的是![]()

A.若A为![]() 溶液,B可能为氨水,反应
溶液,B可能为氨水,反应![]() 的离子方程式为:
的离子方程式为:![]()
B.若A为Fe,B可能为稀硝酸,反应![]() 的离子方程式为:
的离子方程式为: ![]()
C.若A为NaOH溶液,B可能为![]() ,可用
,可用![]() 溶液鉴别C、D溶液
溶液鉴别C、D溶液
D.若A为![]() ,B可能为
,B可能为![]() ,实验室可用加热固体C的方法制取
,实验室可用加热固体C的方法制取![]()
【答案】B
【解析】
A.氯化铝与氨水只能生成白色沉淀![]() ,氢氧化铝不能与氨水继续反应生成偏铝酸钠,故A错误;
,氢氧化铝不能与氨水继续反应生成偏铝酸钠,故A错误;
B.Fe粉与少量硝酸反应生成的![]() 与过量的铁继续反应生成
与过量的铁继续反应生成![]() ,故B正确;
,故B正确;
C.若A为NaOH溶液,B可能为![]() ,则C为
,则C为![]() ,D为
,D为![]() ,二者遇到氢氧化钙均生成白色沉淀,不能用氢氧化钙鉴别,故C错误;
,二者遇到氢氧化钙均生成白色沉淀,不能用氢氧化钙鉴别,故C错误;
D.直接加热氯化铵,氯化铵分解生成氨气和HCl,在试管口处又化合生成氯化铵,不能制取氨气,故D错误。
故选B。

【题目】下列有关实验操作、发生的现象、解释或结论都正确的是![]()
选项 | 实验操作 | 发生现象 | 解释或结论 |
A | 向NaCl和KI的混合溶液中,逐滴加入 | 溶液中先产生白色沉淀,后产生黄色沉淀 |
|
B | 用玻璃棒蘸取氯水点到蓝色石蕊试纸上 | 试纸先变红后褪色 | 氯水中含有 |
C | 将铜片与芯片用导线连接后,插入稀硫酸中 | 铜片上有气泡产生 | 在锌的作用下,铜与硫酸反应产生氢气 |
D | 向某溶液中加入过量盐酸 | 产生能使澄清石灰水变浑浊的无色气体 | 该溶液为 |
A.AB.BC.CD.D
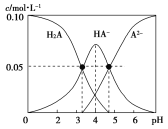
【题目】电离能是衡量元素失电子能力的重要依据,随着元素核电荷数的递增,电离能值呈现周期性变化规律。根据所学知识,回答下列问题。
![]() 第一电离能指的是______。
第一电离能指的是______。
![]() 如图是部分元素原子的第一电离能
如图是部分元素原子的第一电离能![]() 随原子序数变化关系
随原子序数变化关系![]() 其中12号至17号元素的有关数据缺失
其中12号至17号元素的有关数据缺失![]() 。
。
![]() 根据图示变化规律,可推测S的第一电离能的大小
根据图示变化规律,可推测S的第一电离能的大小![]() 最小
最小![]() 范围为______
范围为______![]() ______
______![]() 填元素符号
填元素符号![]() 。
。
![]() 据图可知,同主族元素原子第一电离能
据图可知,同主族元素原子第一电离能![]() 变化规律是______。
变化规律是______。
![]() 图中第一电离能最小的元素在周期表中的位置______。
图中第一电离能最小的元素在周期表中的位置______。
![]() 根据对角线规则铍元素最高价氧化物的水化物应该具有______。
根据对角线规则铍元素最高价氧化物的水化物应该具有______。
![]() 用In表示元素的第n电离能,则图中的a、b、c分别代表______。
用In表示元素的第n电离能,则图中的a、b、c分别代表______。

A.a为![]() 、b为
、b为![]() 、c为
、c为![]()
B.a为![]() 、b为
、b为![]() 、c为
、c为![]()
C.a为![]() 、b为
、b为![]() 、c为
、c为![]() D.a为
D.a为![]() 、b为
、b为![]() 、c为
、c为![]()
![]() 铜、锌两种元素的第一电离能、第二电离能如表所示:
铜、锌两种元素的第一电离能、第二电离能如表所示:
电离能 |
|
|
Cu | 746 | 1958 |
Zn | 906 | 1733 |
铜的第一电离能![]() 小于锌的第一电离能,而铜的第二电离能
小于锌的第一电离能,而铜的第二电离能![]() 却大于锌的第二电离能,其主要原因是______。
却大于锌的第二电离能,其主要原因是______。
![]() 与电离能的定义相类似,元素的气态基态原子得到一个电子形成气态负一价阴离子时所放出的能量称作第一电子亲和能
与电离能的定义相类似,元素的气态基态原子得到一个电子形成气态负一价阴离子时所放出的能量称作第一电子亲和能![]() ,负一价阴离子再获得一个电子的能量变化叫做第二电子亲和能
,负一价阴离子再获得一个电子的能量变化叫做第二电子亲和能![]() ,部分元素或离子的电子亲和能数据如下表所示:
,部分元素或离子的电子亲和能数据如下表所示:
元素 | Cl | Br | I | O |
|
电子亲和能 | 349 | 343 | 295 | 141 |
|
![]() 下列说法中错误的是______。
下列说法中错误的是______。
A.元素的电子亲和能越大,越容易得到电子
B.一个基态的气态氧原子得到一个电子成为![]() 时放出141kJ的能量
时放出141kJ的能量
C.氧元素的第二电子亲和能是![]()
D.基态的气态氧原子得到两个电子成为![]() 需要吸收能量
需要吸收能量
![]() 图中数据显示,同主族元素
图中数据显示,同主族元素![]() 从上到下依次减小,其原因是_____。
从上到下依次减小,其原因是_____。