题目内容
下列离子方程式书写正确的是( )
| A、少量的CO2通入氨水中:CO2+NH3?H2O=NH4++HCO3- |
| B、将Na2CO3溶液逐滴滴入盐酸中:2H++CO32-=CO2↑+H2O |
| C、SO2使紫色石蕊溶液变红色:SO2+H2O?2H++SO32- |
| D、足量铁粉与稀硝酸反应:Fe+4H++NO3-=Fe3++2H2O+NO↑ |
考点:离子方程式的书写
专题:
分析:A.反应生成碳酸铵;
B.盐酸过量,生成氯化钠、水、二氧化碳;
C.二氧化硫与水反应生成亚硫酸,亚硫酸电离分步进行,以第一步为主;
D.铁过量,则生成硝酸亚铁.
B.盐酸过量,生成氯化钠、水、二氧化碳;
C.二氧化硫与水反应生成亚硫酸,亚硫酸电离分步进行,以第一步为主;
D.铁过量,则生成硝酸亚铁.
解答:
解:A.少量的CO2通入氨水中的离子反应为CO2+2NH3?H2O=2NH4++CO32-+H2O,故A错误;
B.将Na2CO3溶液逐滴滴入盐酸中的离子反应为2H++CO32-=CO2↑+H2O,故B正确;
C.SO2使紫色石蕊溶液变红色的离子反应为SO2+H2O?H2SO3?H++HSO3-,故C错误;
D.足量铁粉与稀硝酸反应的离子反应为3Fe+8H++2NO3-=3Fe2++4H2O+2NO↑,故D错误;
故选B.
B.将Na2CO3溶液逐滴滴入盐酸中的离子反应为2H++CO32-=CO2↑+H2O,故B正确;
C.SO2使紫色石蕊溶液变红色的离子反应为SO2+H2O?H2SO3?H++HSO3-,故C错误;
D.足量铁粉与稀硝酸反应的离子反应为3Fe+8H++2NO3-=3Fe2++4H2O+2NO↑,故D错误;
故选B.
点评:本题考查离子反应方程式书写的正误判断,为高考经典题型,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、与量有关的离子反应的考查,题目难度不大.

练习册系列答案
相关题目
“富勒烯”家族又增添了新成员,继C60、C70、N60之后,中美科学家首次发现了全硼富勒烯B40.下列说法正确的是( )
| A、B40和C70、都属于新型化合物 |
| B、C60、和N60属于同分异构体 |
| C、B40、C60、N60、C70都只含共价键 |
| D、B40、C60、N60、C70都属于烯烃 |
下列反应中,不能用离子方程式 SO42-+Ba2+=BaSO4↓来表示的是( )
| A、稀硫酸与硝酸钡溶液反应 |
| B、硫酸钾溶液与氯化钡溶液反应 |
| C、稀硫酸与氢氧化钡溶液反应 |
| D、硫酸钠溶液与硝酸钡溶液反应 |
有关下列四个常用电化学装置的叙述中,正确的是( )
 |  | 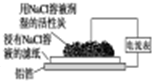 |  |
| 图Ⅰ碱性 锌锰电池 | 图Ⅱ铅硫 酸蓄电池 | 图Ⅲ铝箔的腐蚀 | 图Ⅳ银锌 纽扣电池 |
| A、图Ⅰ所示电池中,MnO2的作用是催化剂,负极反应为:Zn-2e-=Zn2+ |
| B、图Ⅱ所示电池充电过程中,硫酸浓度不断增大,阴极反应为:Pb+SO42-=PbSO4-2e- |
| C、铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl--2e-═Cl2↑ |
| D、图Ⅳ所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag |






 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g) 某探究活动小组想利用原电池反应检测金属的活动性顺序,有甲、乙两位同学均使用镁片与铝片作电极,但甲同学将电极放入6mol?L-1稀H2SO4中,乙同学将电极放入6mol?L-1的NaOH溶液中,如图所示.
某探究活动小组想利用原电池反应检测金属的活动性顺序,有甲、乙两位同学均使用镁片与铝片作电极,但甲同学将电极放入6mol?L-1稀H2SO4中,乙同学将电极放入6mol?L-1的NaOH溶液中,如图所示.