题目内容
下列说法错误的是( )
| A.气态电中性基态原子失去电子转化为气态基态正离子需要的最低能量叫做第一电离能 |
B.当碳原子的核外电子排布由 转变为 转变为  时,碳原子要向外界环境吸收能量 时,碳原子要向外界环境吸收能量 |
| C.电负性的大小也可以作为判断金属性和非金属性强弱的尺度 |
| D.同主族元素从上到下第一电离能逐渐变小 |
A
解析试题分析:气态电中性基态原子失去一个电子转化为气态基态正离子需要的最低能量叫做第一电离能,A错误。B中碳原子从基态变为激发态,需要向外界吸收能量,B正确。电负性的大小可以作为判断金属性和非金属性强弱的尺度,C正确。同主族元素从上到下,最外层电子数相同,而原子半径逐渐增大,所以第一电离能逐渐变小,D正确。
考点:电离能
点评:本题主要考查电离能的概念及应用,属于概念性理解,难度不大,侧重考查学生对概念的理解程度,细心程度。

练习册系列答案
相关题目
如表是不同pH环境时某浓度铬酸(H2CrO4)溶液中,离子浓度(mol/L)与pH的关系,下列说法错误的是( )
|
如图为元素周期表中短周期的一部分,下列说法错误的是( )
| X | Y |
| Z | W |
| A、Z的原子序数可能是X的两倍 |
| B、单质的活泼性可能是Y<Z |
| C、X、Z的最高价氧化物对应水化物可能均为强酸 |
| D、分别由Y、W形成的单质可能都是原子晶体 |
化学反应原理中涉及很多常数,下列说法错误的是( )
A、反应N2(g)+3H2(g)
| |||||
| B、化学平衡常数、弱电解质的电离平衡常数、溶度积常数均只受温度的影响 | |||||
| C、对于弱电解质的电离平衡常数,当温度一定时,电离平衡常数越小,其酸性越强 | |||||
| D、将AgNO3溶液和KCl溶液混合后,若c(Ag+)?c(Cl-)<KSP(AgCl),则溶液中无沉淀生成 |
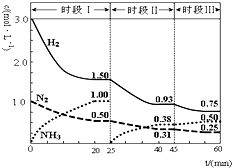 N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1.1L密闭恒容容器中,反应体系中各物质浓度随时间变化的曲线如图示.下列说法错误的是( )
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1.1L密闭恒容容器中,反应体系中各物质浓度随时间变化的曲线如图示.下列说法错误的是( )| A、前20分钟反应物的转化率为50% | B、第25分钟改变的条件是将NH3从反应体系中分离出去 | C、时段Ⅰ仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数增大 | D、若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度 |