题目内容
常温下,下列各组离子在制定溶液中一定能大量共存的是( )
| A、使苯酚显紫色的溶液:NH4+、K+、SCN-、NO3- |
| B、加入铝粉产生氢气的溶液:Na+、K+、SO42-、Cl- |
| C、c(C6H5OH)=0.1mol?L-1的溶液中:K+、HCO3-、SO42-、CO32- |
| D、由水电离产生的c(H+)=10-13mol?L-1的溶液:Fe2+、Na+、NO3-、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:A.使苯酚显紫色的溶液,含Fe3+,离子之间结合生成络离子;
B.加入铝粉产生氢气的溶液,为非氧化性酸或强碱溶液;
C.C6H5OH与CO32-反应;
D.由水电离产生的c(H+)=10-13mol?L-1的溶液,为酸或碱溶液.
B.加入铝粉产生氢气的溶液,为非氧化性酸或强碱溶液;
C.C6H5OH与CO32-反应;
D.由水电离产生的c(H+)=10-13mol?L-1的溶液,为酸或碱溶液.
解答:
解:A.使苯酚显紫色的溶液,含Fe3+,与SCN-结合生成络离子,不能共存,故A错误;
B.加入铝粉产生氢气的溶液,为非氧化性酸或强碱溶液,酸、碱溶液中该组离子之间均不反应,可大量共存,故B正确;
C.C6H5OH与CO32-反应,不能共存,故C错误;
D.由水电离产生的c(H+)=10-13mol?L-1的溶液,为酸或碱溶液,酸溶液中Fe2+、H+、NO3-发生氧化还原反应,碱溶液中不能存在Fe2+,故D错误;
故选B.
B.加入铝粉产生氢气的溶液,为非氧化性酸或强碱溶液,酸、碱溶液中该组离子之间均不反应,可大量共存,故B正确;
C.C6H5OH与CO32-反应,不能共存,故C错误;
D.由水电离产生的c(H+)=10-13mol?L-1的溶液,为酸或碱溶液,酸溶液中Fe2+、H+、NO3-发生氧化还原反应,碱溶液中不能存在Fe2+,故D错误;
故选B.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子的反应为解答的关键,侧重分析能力与氧化还原反应、络合反应的考查,题目难度不大.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
下列离子方程式正确的是( )
| A、铁和硫酸铜溶液反应:Fe+Cu2+═Cu+Fe2+ |
| B、氢氧化铜与硫酸溶液反应:OH-+H+═H2O |
| C、碳酸钙与盐酸溶液反应:CO32-+2H+═H2O+CO2↑ |
| D、铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
对于已经达到平衡的可逆反应,下列物理量的变化可以肯定可逆反应平衡发生了移动的是( )
| A、浓度变化 | B、压强变化 |
| C、体积变化 | D、转化率变化 |
扑热息痛是一种优良的解热镇痛剂其结构为 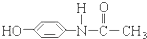 它可能具有的化学性质是( )
它可能具有的化学性质是( )
 它可能具有的化学性质是( )
它可能具有的化学性质是( )| A、不与烧碱溶液反应 |
| B、能与溴水发生取代反应 |
| C、不能被氧化 |
| D、遇FeCl3溶液发生显色反应 |
下列醇中能由醛加氢还原制得的是( )
| A、CH3CH2CH2OH |
| B、(CH3) 2CHCH(CH3) OH |
| C、(CH3) 3COH |
| D、(CH3) 2CHOH |
下列对聚丙烯的描述有错误的是( )
| A、聚丙烯的分子长链是由C-C键连接而成的 |
| B、聚丙烯分子的长链上有支链 |
| C、聚丙烯每个链节内含3个碳原子 |
| D、聚丙烯能使溴水褪色 |
下列说法不正确的是( )
| A、△H<0且熵增大的反应一定可以自发进行 |
| B、△H>0且熵减小的反应一定不能自发进行 |
| C、△H>0且熵增大的反应一定可以自发进行 |
| D、△H<0且熵减小的反应有可能可以自发进行 |
下列变化中,属于还原反应的是( )
| A、Fe→FeSO4 |
| B、Cu(NO3)2→Cu |
| C、P→P2O5 |
| D、NaCl→AgCl |
