题目内容
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、常温常压下,18 g H2O分子中含有的原子总数为3NA |
| B、标准状况下,11.2 L乙醇中含有分子的数目为0.5NA |
| C、常温常压下,2.24 LCO2中含有的C原子数目为0.1NA |
| D、标准状况下,分子数为NA的氧气和氮气的混合气体所占的体积为44.8 L |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.质量转化成物质的量结合分子的构成解答;
B.气体摩尔体积适用对象为气体;
C.常温常压下Vm≠22.4L/mol;
D.标况下1mol任何气体所占体积为22.4L.
B.气体摩尔体积适用对象为气体;
C.常温常压下Vm≠22.4L/mol;
D.标况下1mol任何气体所占体积为22.4L.
解答:
解:A.1个水分子含有2个氢原子和1个氧原子,18 g H2O的物质的量=
=1mol,含有的原子总数为3NA,故A正确;
B.标准状况下,乙醇为液体,不能使用气体摩尔体积,故B错误;
C.常温常压下Vm≠22.4L/mol,2.24 LCO2的物质的量不为1mol,故C错误;
D.分子数为NA的氧气和氮气物质的量为1mol,标况下1mol任何气体所占体积为22.4L,故D错误;
故选:A.
| 18g |
| 18g/mol |
B.标准状况下,乙醇为液体,不能使用气体摩尔体积,故B错误;
C.常温常压下Vm≠22.4L/mol,2.24 LCO2的物质的量不为1mol,故C错误;
D.分子数为NA的氧气和氮气物质的量为1mol,标况下1mol任何气体所占体积为22.4L,故D错误;
故选:A.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件应用分析,质量换算物质的量计算微粒数,微粒结构特征分析,掌握基础是关键,题目难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
下列解释正确的是( )
| A、摩尔是国际七个基本物理量之一 |
| B、物质的量是一个独立的专有名词 |
| C、摩尔是物质的质量的单位 |
| D、摩尔质量等于相对分子质量 |
将含有硝酸钙和硫酸镁杂质的硝酸钾溶于水,加入某些试剂,结合过滤、蒸发等操作,可得到纯净的硝酸钾.加入试剂的顺序正确的是( )
| A、K2CO3、Ba(NO3)2、KOH、HNO3 |
| B、Ba(NO3)2、KOH、HNO3、K2CO3 |
| C、KOH、K2CO3、Ba(NO3)2、HNO3 |
| D、Ba(NO3)2、KOH、K2CO3、HNO3 |
对于某些离子的检验及结论一定正确的是( )
| A、加入稀盐酸产生气体,将气体通入澄清石灰水,溶液变浑浊,可能有CO32- |
| B、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| C、加硝酸银溶液产生白色沉淀,一定有Cl- |
| D、加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
除去混合物中的杂质(括号中为杂质),所选试剂和分离方法都正确的是( )
| 混合物 | 除杂试剂 | 分离方法 | |
| A | 溴苯(溴) | NaOH溶液 | 分液 |
| B | 乙烷(乙烯) | 酸性KMnO4 | 洗气 |
| C | 甲苯(苯酚) | 溴水 | 过滤 |
| D | 溴乙烷(乙醇) | NaOH溶液 | 分液 |
| A、A | B、B | C、C | D、D |
在下列变化中,需要加入合适的氧化剂才能实现的是( )
| A、Na2O2→O2 |
| B、CO2→CO |
| C、Fe2O3→Fe |
| D、Br-→Br2 |
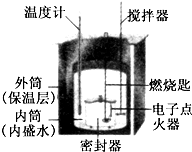 某化学兴趣小组将两份等质量的硫粉分别在空气、氧气中燃烧,放出的热量是一样多还是不一样多?经过讨论、综合,根据观点分成了两组.
某化学兴趣小组将两份等质量的硫粉分别在空气、氧气中燃烧,放出的热量是一样多还是不一样多?经过讨论、综合,根据观点分成了两组.