题目内容
(4分)冶炼金属的三种常用方法是:①热分解法 ②热还原剂法 ③电解法。人类用量处在前三位的金属是铁、铝、铜。(填编号)
(1)冶炼铝用到的方法是 ;(2)冶炼铁和铜的常用方法是 。
【答案】
③ ②
【解析】一般不活泼的金属,可以直接用加热分解的方法从其化合物中还原出来。非常活泼的金属,常用电解法冶炼。大部分金属的冶炼都是通过高温下利用还原剂C、CO、氢气等还原出来。所以冶炼铝是电解法,铁和铜是还原剂法。

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
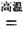 TiCl4+2CO
TiCl4+2CO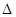 H=-393.5 kJ·mol-1
H=-393.5 kJ·mol-1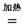 4NaCl+Ti,该反应不能在水溶液中进行,一是因为TiCl4会强烈水解生成TiO2,另一原因
(用适当化学方程式辅以必要的文字说明)。
4NaCl+Ti,该反应不能在水溶液中进行,一是因为TiCl4会强烈水解生成TiO2,另一原因
(用适当化学方程式辅以必要的文字说明)。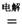 Mg+Cl2
TiCl4+2Mg
Mg+Cl2
TiCl4+2Mg 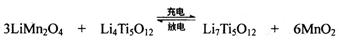 ,使用时先充电,写出其充电式的阳极反应 ,放电时Li+的移动方向
。
,使用时先充电,写出其充电式的阳极反应 ,放电时Li+的移动方向
。