题目内容
6.下列各组物项相互混合进行反应,既有气体生成最终又有沉淀生成的是( )①金属钠投入FeCl2溶液中
②过量的NaOH溶液和明矾溶液反应
③少量CaO投入过量的NaHCO3溶液中
④Na2O2投入到CuSO4溶液中.
| A. | ①③ | B. | ③④ | C. | ①④ | D. | ②③ |
分析 ①中Na与FeCl2溶液反应生成Fe(OH)2沉淀和H2;
②中过量的NaOH溶液和KAl(SO4)2溶液反应,一方面使Al3+变为AlO2-,即无沉淀产生,另一方面也无气体生成;
③中CaO与NaHCO3溶液反应生成CaCO3沉淀;
④中Na2O2与CuSO4溶液反应生成Cu(OH)2沉淀和O2;
解答 解:①钠浮在水面上,与水剧烈反应,并放出大量热,熔化成小球,黄色的溶液变成红色沉淀,发生2Na+H2O=2NaOH+H2↑、3NaOH+FeCl3=3NaCl+Fe(OH)3↓,故①既有气体生成最终又有沉淀生成;
②过量的NaOH溶液和明矾溶液反应的方程式为:KAl(SO4)2•12H2O+4NaOH=KAlO2+14H2O+2Na2SO4,故②中既无气体生成最终又无沉淀生成;
③中CaO与NaHCO3溶液反应生成CaCO3沉淀;,故③最终只有沉淀生成;
④Na2O2与水反应:2Na2O2+2H2O=4NaOH+O2↑,NaOH与CuSO4发生反应:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4,故④中既有气体生成最终又有沉淀生成;
故选C.
点评 该题主要考查了元素钠、铝、硫、铁的化合物的性质,要求掌握这些化合物的一些重要的化学反应方程式,并理解为什么会发生,从而运用这些反应解相关的问题.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
17.强酸和强碱的稀溶液的中和热可表示为:H+(aq)+OH-(aq)═H2O(1);△H=-57.3kJ/mol.已知:
CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(1);△H=-Q1kJ/mol
$\frac{1}{2}$H2SO4(浓)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(1);△H=-Q2kJ/mol
HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(1);△H=-Q3kJ/mol
则Q1、Q2、Q3的关系正确的是( )
CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(1);△H=-Q1kJ/mol
$\frac{1}{2}$H2SO4(浓)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(1);△H=-Q2kJ/mol
HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(1);△H=-Q3kJ/mol
则Q1、Q2、Q3的关系正确的是( )
| A. | Q3>Q2>Q1 | B. | Q1>Q3>Q2 | C. | Q1=Q2=Q3 | D. | Q2>Q3>Q1 |
18.(1)A和B反应生成C,假定反应由A、B开始,它们的起始浓度均为1mol•L-1.反应进行2min后A的浓度为0.8mol•L-1,B的浓度为0.6mol•L-1,C的浓度为0.6mol•L-1.则2min内反应的平均速v(A)=0.1mol/(Lmin).
(2)反应A+3B═2C+2D在四种不同情况下的反应速率分别为:
①v(A)=0.15mol•L-1•s-1
②v(B)=0.6mol•L-1•s-1
③v(C)=0.4mol•L-1•s-1
④v(D)=0.45mol•L-1•s-1.
该反应进行的快慢顺序为④>②=③>①
(3)如表是稀硫酸与某金属反应的实验数据:
分析上述数据,回答下列问题:
?实验4和5表明,固体反应物的表面积对反应速率有影响,表面积越大 反应速率越快,能表明同一规律的实验还有1和2(填实验序号);?本实验中影响反应速率的其他因素还有反应温度,其实验序号是6和7、8和9.
(2)反应A+3B═2C+2D在四种不同情况下的反应速率分别为:
①v(A)=0.15mol•L-1•s-1
②v(B)=0.6mol•L-1•s-1
③v(C)=0.4mol•L-1•s-1
④v(D)=0.45mol•L-1•s-1.
该反应进行的快慢顺序为④>②=③>①
(3)如表是稀硫酸与某金属反应的实验数据:
| 实验序号 | 金属 质量/g | 金属状态 | c(H2SO4) /mol•L-1 | V(H2SO4) /mL | 溶液温度/℃ | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | 丝 | 0.7 | 50 | 20 | 36 | 250 |
| 4 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
| 6 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
| 7 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
| 8 | 0.10 | 丝 | 1.1 | 50 | 20 | 34 | 100 |
| 9 | 0.10 | 丝 | 1.1 | 50 | 30 | 44 | 40 |
?实验4和5表明,固体反应物的表面积对反应速率有影响,表面积越大 反应速率越快,能表明同一规律的实验还有1和2(填实验序号);?本实验中影响反应速率的其他因素还有反应温度,其实验序号是6和7、8和9.
1.已知丁烷有两种同分异构体,则分子式为C4H9Cl的有机物共有(不考虑立体异构)( )
| A. | 7种 | B. | 6种 | C. | 5种 | D. | 4种 |
11.化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A. | 氢氧燃料电池在碱性介质中的负极反应式:O2+2H2O+4e-=4OH- | |
| B. | 电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-=Cl2↑ | |
| C. | 粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ | |
| D. | 钢铁发生电化学腐蚀的正极反应式:Fe-2e-=Fe2+ |
16.钛和钛合金在航空工业有重要应用.冶炼钛的过程中发生的反应之一为TiO2+2C+2Cl2═TiCl4+2CO.对此,下列说法错误的是( )
| A. | C是还原剂 | |
| B. | TiO2是氧化剂 | |
| C. | 生成1 mol TiCl4时,转移电子4 mol | |
| D. | 尾气必须净化处理 |
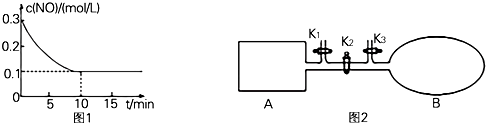

 (其中:-X、-Y均为官能团
(其中:-X、-Y均为官能团 .
.