题目内容
下列元素按电负性由大到小顺序排列的是 ( )(填标号)
| A、K、Na、Li | B、N、O、F | C、As、P、N | D、Cl、S、C |
分析:同一周期元素中,元素的电负性随着原子序数的增大而增大,同一主族中,元素的电负性随着原子序数的增大而减弱,所以元素的非金属性越强,其电负性越大,元素的金属性越强,其电负性越小,据此分析解答.
解答:解:A.K、Na、Li为同一主族元素,且元素的原子序数逐渐减小,其电负性逐渐增大,故A错误;
B.N、O、F属于同一主族,其原子序数逐渐增大,所以其电负性随着原子序数的增大而增大,故B错误;
C.As、P、N元素属于同一主族元素,其原子序数逐渐减小,则其电负性逐渐增大,故C错误;
D.Cl、S、C元素的非金属性逐渐减弱,则其电负性逐渐减小,故D正确;
故选D.
B.N、O、F属于同一主族,其原子序数逐渐增大,所以其电负性随着原子序数的增大而增大,故B错误;
C.As、P、N元素属于同一主族元素,其原子序数逐渐减小,则其电负性逐渐增大,故C错误;
D.Cl、S、C元素的非金属性逐渐减弱,则其电负性逐渐减小,故D正确;
故选D.
点评:本题考查了电负性大小的判断,根据元素的非金属性与电负性的关系是解本题关键,结合元素周期律来分析解答,难度不大.

练习册系列答案
相关题目
 ,具有抗癌作用;反铂的结构式为
,具有抗癌作用;反铂的结构式为 ,无抗癌作用。
,无抗癌作用。
 (3)乙二胺分子中氮原子轨道的杂化类型为_____________。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是_______________________________________。
(3)乙二胺分子中氮原子轨道的杂化类型为_____________。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是_______________________________________。



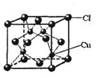
 (4)②中所形成的配离子中含有的化学键类型有__________。(填字母)
(4)②中所形成的配离子中含有的化学键类型有__________。(填字母)


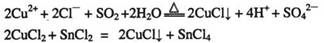

 (3)乙二胺分子中氮原子轨道的杂化类型为_____________。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是_______________________________________。
(3)乙二胺分子中氮原子轨道的杂化类型为_____________。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是_______________________________________。