题目内容
有一包白色粉末,其中可能由K2CO3、、CaCl2、Ba(NO3)2,为检验它们,做了如下实验:
①将部分粉末溶于水,振荡,有白色沉淀生成;
②向①的悬浊液中加入过量稀硝酸,有白色沉淀消失,并有气泡产生;
③取少量②的溶液滴入AgNO3溶液,有白色沉淀生成.
根据上述实验现象,判断原白色粉末中肯定含有什么物质,可能含有什么物质试判断:
(1)原白色粉末中肯定有________,可能有________;(用化学式填写)
(2)写有关反应的离子方程式:________,________,________.
答案:
解析:
解析:
|
(1)原白色粉末中肯定有K2CO3、CaCl2,可能有Ba(NO3)2;(用化学式填写) (2)写有关反应的离子方程式:CO32-+Ca2+=CaCO3↓ CaCO3+2H+=Ca2++CO2↑+H2O Ag++Cl-=AgCl↓. |

练习册系列答案
相关题目
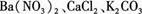 ,现做以下实验。
,现做以下实验。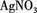 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。 现象,判断白色粉末中一定含有 (填化学式),可能含自 (填化学式)。写出(3)中有关反应的离子方程式 。
现象,判断白色粉末中一定含有 (填化学式),可能含自 (填化学式)。写出(3)中有关反应的离子方程式 。