题目内容
12.有以下微粒:${\;}_{8}^{16}$O、${\;}_{20}^{40}$Ca、${\;}_{8}^{18}$O、${\;}_{7}^{14}$N、${\;}_{17}^{37}$Cl、${\;}_{18}^{40}$Ar,其中(1)互为同位素的是${\;}_{8}^{16}$O 和${\;}_{8}^{18}$O
(2)质量数相等,但不能互称同位素的是4020Ca 和4018Ar
(3)中子数相等,但质子数不等的是${\;}_{20}^{40}$Ca 和${\;}_{17}^{37}$Cl
(4)写出上述微粒中最高价氧化物对应的水化物碱性最强的碱与最高价氧化物对应的水化物酸性最强的酸反应的化学方程式2HClO4+Ca(OH)2=Ca(ClO4)2+2H2O.
分析 (1)质子数相同,中子数不同的同种元素的不同原子互为同位素;
(2)质量数=质子数+中子数;
(3)中子数=质量数-质子数;
(4)根据元素周期律:周期表中从左到右失电子能力逐渐减弱,得电子能力逐渐增强,元素非金属性逐渐增强,从上到下失电子能力逐渐增强,得电子能力逐渐减弱,元素非金属性逐渐减弱.
解答 解:(1)同位素是指具有相同的质子数而中子数不同的同一元素的不同核素之间的互称,上述微粒属于同种元素的只有${\;}_{8}^{16}$O;${\;}_{8}^{18}$O,所以互为同位素的是${\;}_{8}^{16}$O;${\;}_{8}^{18}$O;故答案为:${\;}_{8}^{16}$O;${\;}_{8}^{18}$O;
(2)在表示原子组成时元素符号的左下角数字表示质子数,左上角数字表示质量数,所以质量数相等,但不能互称同位素的是4020Ca 和 4018Ar;故答案为:4020Ca、4018Ar;
(3)根据质子数+中子数=质量数,4020Ca中中子数=40-20=20、${\;}_{17}^{37}$Cl中中子数=37-17=20,所以中子数相等,但质子数不相等的是4020Ca和${\;}_{17}^{37}$Cl,故答案为:4020Ca;${\;}_{17}^{37}$Cl;
(4)上述元素中Cl的非金属性最强,则最高价氧化物对应的水化物的酸性最强,该酸为HClO4,Ca的金属性最强,则Ca(OH)2的碱性最强,反应的方程式:2HClO4+Ca(OH)2=Ca(ClO4)2+2H2O,故答案为:2HClO4+Ca(OH)2=Ca(ClO4)2+2H2O.
点评 本题主要考查的是同位素的概念,原子核内质子数、中子数和质量数的关系,难度不大,判断元素的非金属性强弱是解题的关键.

①I2(g)浓度减小 ②混合气颜色变浅 ③I2(g)转化率增大 ④HI(g)质量分数增大 ⑤I2(g)+H2(g)质量分数减小.
| A. | ①②③ | B. | ②③④ | C. | ③④⑤ | D. | ①③⑤ |
| A. | 5.6 g铁粉在0.1 mol氯气中充分燃烧,转移电子数为0.3NA | |
| B. | 7.8 g Na2S和Na2O2中含有的阴离子数大于0.1NA | |
| C. | 56 g铁片投入足量浓硫酸中生成NA个SO2分子 | |
| D. | 常温常压下,46 g的NO2和N2O4混合气体含有的原子数为3NA |
| A. | Cl2+2I-→2Cl-+I2 | B. | 酸性:HClO3>HIO3 | C. | 酸性:HClO4>HIO4 | D. | 稳定性:HCl>HI |
| A. |  向含有H+,Al3+,Mg2+的溶液中,逐渐加入NaOH溶液 | |
| B. |  向Al2(SO4)3溶液中加入Ba(OH)2溶液 | |
| C. |  物质的量相等的镁和铝分别与等浓度、等体积的过量稀硫酸反应 | |
| D. |  向AlCl3溶液中加氨水 |
| A. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | B. | 2CH2CH2OH$→_{△}^{Cu}$2CH3CHO+H2O | ||
| C. | CH4+Cl2$\stackrel{光}{→}$CH2Cl+HCl | D. | CH2═CH2+H2$\stackrel{催化剂}{→}$CH3-CH3 |
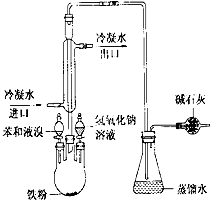 如图是实验室制取溴苯的装置图
如图是实验室制取溴苯的装置图