题目内容
7.2.2gD${\;}_{2}^{18}$O中所含中子和质子的物质的量分别为1.2mol、1mol.分析 D218O中质子数=电子数=2+8=10,中子数=2+10=12,结合n=$\frac{m}{M}$计算2.2gD218O的物质的量,然后计算出所含中子和质子的物质的量.
解答 解:D218O中质子数=2+8=10,中子数=2+10=12,
2.2gD218O的物质的量为:n(D218O)=$\frac{2.2g}{22g/mol}$=0.1mol,
0.1molD218O含有中子的物质的量为:0.1mol×12=1.2mol;
0.1molD218O含有质子的物质的量为:0.1mol×10=1mol,
故答案为:1.2mol;1mol.
点评 本题考查了物质的量的计算,题目难度不大,明确质量数与质子数、中子数的关系为解答关键,注意掌握物质的量与摩尔质量之间的关系,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
2.下列有关化学用语使用正确的是( )
| A. | CO2的球棍模型: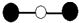 | B. | 乙烷的结构式CH3-CH3 | ||
| C. | 新戊烷的结构简式:C(CH3)4 | D. | CCl4的电子式: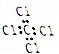 |
4.下列关于材料的说法错误的是( )
| A. | 羊毛的主要成分是纤维素 | B. | 塑料属于合成材料 | ||
| C. | 普通玻璃属于硅酸盐材料 | D. | 不锈钢属于合金 |
11.汽车轮胎的主要成分是( )
| A. | 塑料 | B. | 纤维 | C. | 复合材料 | D. | 橡胶 |
9.影响金属冶炼方法的主要因素是( )
| A. | 金属的活动性大小 | B. | 金属在地壳中的含量多少 | ||
| C. | 金属的化合价高低 | D. | 金属的导电性强弱 |
