题目内容
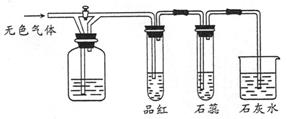
下图所示装置中,若关闭活塞,则品红溶液无变化,石蕊溶液变红,石灰水变浑浊。据此判断气体和广口瓶中盛放的物质是
- A.SO2和H2SO4(浓)
- B.SO2和饱和NaHCO3
- C.Cl2和NaHSO3
- D.NO2和KOH
B
试题分析:关闭活塞,则品红溶液无变化,石蕊溶液变红,石灰水变浑浊,这说明无色气体中一定含有CO2或提高洗气瓶中有CO2生成。A中浓硫酸不能吸收SO2,品红溶液褪色,不符合题意;B中通入饱和NaHCO3溶液后发生反应:SO2+NaHCO3═Na2SO3+2CO2↑+H2O,SO2被吸收而放出CO2,所以品红溶液无变化,石蕊溶液变红,石灰水变浑浊,,符合题意;C中氯气是黄绿色气体,且具有强氧化性,能把亚硫酸氢钠氧化生成硫酸钠,没有气体溢出,不符合题意;D中NO2是红棕色气体,通入到KOH溶液中NO2被吸收,,没有气体溢出,不符合题意,答案选B。
考点:考查SO2、氯气和NO2以及CO2的性质、物质的检验
点评:该题是中等难度的试题,侧重对学生实验能力的培养,有助于培养学生分析、归纳和总结问题的能力。本题根据现象来推测物质,然后再进行一一验证,这也是解决问题的一种方法,需要学生注意总结、归纳和应用。
试题分析:关闭活塞,则品红溶液无变化,石蕊溶液变红,石灰水变浑浊,这说明无色气体中一定含有CO2或提高洗气瓶中有CO2生成。A中浓硫酸不能吸收SO2,品红溶液褪色,不符合题意;B中通入饱和NaHCO3溶液后发生反应:SO2+NaHCO3═Na2SO3+2CO2↑+H2O,SO2被吸收而放出CO2,所以品红溶液无变化,石蕊溶液变红,石灰水变浑浊,,符合题意;C中氯气是黄绿色气体,且具有强氧化性,能把亚硫酸氢钠氧化生成硫酸钠,没有气体溢出,不符合题意;D中NO2是红棕色气体,通入到KOH溶液中NO2被吸收,,没有气体溢出,不符合题意,答案选B。
考点:考查SO2、氯气和NO2以及CO2的性质、物质的检验
点评:该题是中等难度的试题,侧重对学生实验能力的培养,有助于培养学生分析、归纳和总结问题的能力。本题根据现象来推测物质,然后再进行一一验证,这也是解决问题的一种方法,需要学生注意总结、归纳和应用。

练习册系列答案
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案
相关题目
有关元素A、B、C、D、E、F的信息如下:
请回答下列问题:
(1)写出物质甲与乙反应的离子方程式______
(2)下列说法不正确的是______(填序号).
①实验室可用右图所示装置制取B的最高价氧化物
②用C单质做成的槽车,可用来运输甲的浓溶液
③C和铜与稀硫酸组成的原电池,C电极被还原
(3)若用石墨做电极电解元素D、E组成的化合物饱和水溶液,写出电解反应的离子方程式为:______
(4)已知:2AO2(g) A2O4(g);△H<0.在恒温恒容条件下,将一定量AO2和A2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示.
A2O4(g);△H<0.在恒温恒容条件下,将一定量AO2和A2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示.
①该反应是由______开始反应的.(填“正反应”、“逆反应”、或“正逆反应同时”.)
②a、b两个点中,表示化学反应处于平衡状态的点是______.
③前10min内用AO2表示的化学反应速率v(AO2)=______mol?L-1?min-1.

| 元 素 | 有关信息 |
| A | 最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐 |
| B | 最外层电子数是次外层电子数的2倍 |
| C | M层上有3个电子 |
| D | 短周期原子半径最大的主族元素 |
| E | 最高正价与最低负价代数和为6 |
(1)写出物质甲与乙反应的离子方程式______
(2)下列说法不正确的是______(填序号).
①实验室可用右图所示装置制取B的最高价氧化物
②用C单质做成的槽车,可用来运输甲的浓溶液
③C和铜与稀硫酸组成的原电池,C电极被还原
(3)若用石墨做电极电解元素D、E组成的化合物饱和水溶液,写出电解反应的离子方程式为:______
(4)已知:2AO2(g)
 A2O4(g);△H<0.在恒温恒容条件下,将一定量AO2和A2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示.
A2O4(g);△H<0.在恒温恒容条件下,将一定量AO2和A2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示.①该反应是由______开始反应的.(填“正反应”、“逆反应”、或“正逆反应同时”.)
②a、b两个点中,表示化学反应处于平衡状态的点是______.
③前10min内用AO2表示的化学反应速率v(AO2)=______mol?L-1?min-1.


 .Na202 b.Na2C03 c.NaHCO3 d.Na2C03和C
.Na202 b.Na2C03 c.NaHCO3 d.Na2C03和C


