题目内容
(14分)Ⅰ.在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,其过程如下图所示,试回答下列问题:
(1)该合成路线对于环境保护的价值在于 。
(2)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂。用离子方程式表示乙醇胺水溶液呈弱碱性的原因 。
(3)CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式: 。
Ⅱ.将燃煤废气中的CO2转化为甲醚的反应原理为:
2CO2(g) + 6H2(g)CH3OCH3(g)+ 3H2O(g)
已知一定压强下,该反应在不同温度、不同投料比时,CO2的转化率见下表:
| 投料比[n(H2) / n(CO2)] | 500 K | 600 K | 700 K | 800 K |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |
(4)该反应的焓变△H 0,熵变△S___0(填>、<或=)。
(5)用甲醚作为燃料电池原料,在碱性介质中该电池负极的电极反应式 。若以1.12 L·min-1(标准状况)的速率向该电池中通入甲醚(沸点为-24.9 ℃),用该电池电解500 mL 2 mol·L-1CuSO4溶液,通电0.50 min后,理论上可析出金属铜 g。
⑴ 有利于防止温室效应
⑵HOCH2CH2NH2 + H2OHOCH2CH2NH3++ OH-]
⑶ CO2(g)+3H2(g)→CH3OH(l)+H2O(l) △H=-131.9kJ/mol(3分)
(4) <(1分),<(1分) (5)CH3OCH3 -12e- +16OH-=2CO32- +11H2O
(6)9.6(3分)
解析:⑵HOCH2CH2NH2 中的-NH2为碱性基团,能结合水电离出的H+,使水的电离平衡正向移动,OH-浓度增大,导致溶液中C(H+)<C(OH-),故乙醇胺水溶液呈弱碱性;
(3)由题意,得下列热化学方程式:
CH3OH(l)+3/2O2(g) →CO2(g)+2H2O(l) △H=-725.5kJ/mol ①
H2(g)+1/2O2(g)→H2O(l) △H=-285.8kJ/mol ②
②×3-①,得:CO2(g)+3H2(g)→CH3OH(l)+H2O(l) △H=-131.9kJ/mol
(4)利用表格中的任同一横行数据分析:温度越高,CO2的转化率越小,即升温,平衡逆向移动,则说明逆向为吸热反应,故正向为放热反应,△H<0;
熵值表示体系的混乱度,该反应中由反应物到生成物气体的体积减小(2+8变到1+3),故体系的混乱度减小,△S<0;
(5)在甲醚燃料电池中,发生甲醚的燃烧反应,而在该反应中甲醚失电子做还原剂,故在碱性介质中负极的电极反应式为CH3OCH3 -12e- +16OH-=2CO32- +11H2O①;
用甲醚燃料电池做电源,电解CuSO4溶液时,回路中电荷守恒,则:
Cu2++2e-=Cu ②
由①②,得:CH3OCH3 -12e-— 6 Cu
1 6
(1.12 L·min-1×0.50 min)/22.4L.mol-1
=0.025mol n(Cu)
故n(Cu)=0.025 mol×6=0.15 mol,m(Cu)= 0.15 mol×64g/mol=9.6g;

 阅读快车系列答案
阅读快车系列答案
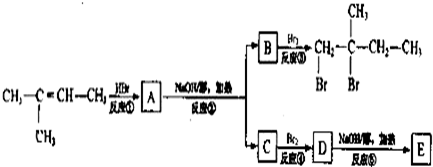
 ),有关反应如下:
),有关反应如下: (2)能说明反应2CH3OH(l)+H2S(g)
(CH3)2S(l) +2H2O(l)达平衡状态的是____________
。
(2)能说明反应2CH3OH(l)+H2S(g)
(CH3)2S(l) +2H2O(l)达平衡状态的是____________
。

 结构的基团,B在HIO4存在并加热时只生成一种产物C,下列为各相关反应的信息和转化关系:
结构的基团,B在HIO4存在并加热时只生成一种产物C,下列为各相关反应的信息和转化关系: