题目内容
一定条件下Cu2O可以和CO发生如下反应:Cu2O(s)+CO(g)?Cu(s)+CO2(g),下列措施中可能使平衡时
增大的是( )
| c(CO) |
| c(CO2) |
分析:A、铜是固体,不影响化学平衡;
B、二氧化碳减少,化学平衡向着正向移动,一氧化碳减少,但是二氧化碳减少的更多;
C、加入一氧化碳,反应前后计量数相等,平衡不移动;
D、改变温度,使反应向着逆向移动,一氧化氮增多,二氧化碳减小.
B、二氧化碳减少,化学平衡向着正向移动,一氧化碳减少,但是二氧化碳减少的更多;
C、加入一氧化碳,反应前后计量数相等,平衡不移动;
D、改变温度,使反应向着逆向移动,一氧化氮增多,二氧化碳减小.
解答:解:A、由于铜粉是固体,基本不影响化学平衡,故A错误;
B、移出一定量的CO2,化学平衡向着正向移动,二氧化碳减少的比一氧化氮减少的多,比值减小,不B错误;
C、加入一氧化氮,由于反应前后气体的计量数相等,化学平衡不移动,比值不变,故C错误;
D、正反应吸热,如升高温度,使反应向着逆向移动,二氧化碳减少,一氧化氮增多,比值增大,故D正确;
故选D.
B、移出一定量的CO2,化学平衡向着正向移动,二氧化碳减少的比一氧化氮减少的多,比值减小,不B错误;
C、加入一氧化氮,由于反应前后气体的计量数相等,化学平衡不移动,比值不变,故C错误;
D、正反应吸热,如升高温度,使反应向着逆向移动,二氧化碳减少,一氧化氮增多,比值增大,故D正确;
故选D.
点评:本题考查了影响化学平衡的影响,根据所学知识完成即可,难度中等.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案
相关题目



 +2Cu(OH)2
+2Cu(OH)2 +Cu2O↓+2H2O
+Cu2O↓+2H2O
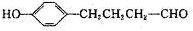 等
等
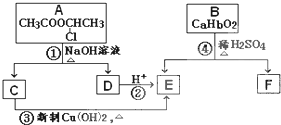
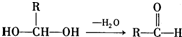
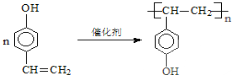
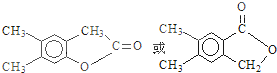
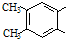 ,它的水解产物经聚合反应后可得到高聚物(CaHbO2)nH有多种结构,写出其中一种的结构简式
,它的水解产物经聚合反应后可得到高聚物(CaHbO2)nH有多种结构,写出其中一种的结构简式