题目内容
|
已知下列热化学方程式:Zn(s)+1/2O2(g)=ZnO(s) ΔH1=-351.1 kJ/mol Hg(l)+1/2O2(g)=HgO(s) ΔH2=-90.7 kJ/mol.由此可知Zn(s)+HgO(s)=ZnO(s)+Hg(l) ΔH3.其中ΔH3的值是 | |
| [ ] | |
A. |
-441.8 kJ/mol |
B. |
-254.6 kJ/mol |
C. |
-438.9 kJ/mol |
D. |
-260.4 kJ/mol |
答案:D

练习册系列答案
相关题目
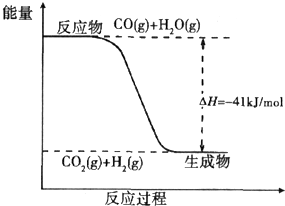 煤炭可以转化为清洁能源和化工原料.
煤炭可以转化为清洁能源和化工原料.