题目内容
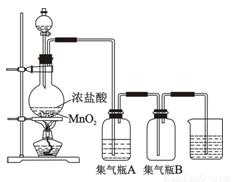
实验室里通常用MnO2与浓盐酸反应制取氯气.现用下列有关装置先制取干燥、纯净的氯气.后进行有关性质实验.试根据下列有关装置回答有关问题.
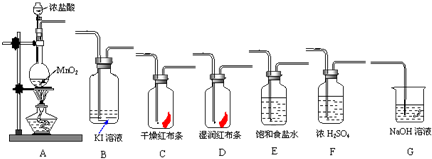
(1)上述装置中各仪器从左至右的连接顺序为A接______接______接______接______接______接G.
(2)E装置的作用是______,D中的现象为______,B中的现象为______
(3)写出相关反应的离子方程式:A中______,B中______,G中______.
(4)在制取氯气的反应:MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O中,如转移电子的物质的量是4mol,则被氧化的HCl的物质的量是______mol,有______ mol Cl2生成.
MnCl2+Cl2↑+2H2O中,如转移电子的物质的量是4mol,则被氧化的HCl的物质的量是______mol,有______ mol Cl2生成.
(5)某温度下,将Cl2通入NaOH溶液中,反应得到含有ClO-与ClO3-物质的量之比为1:1的混合液,反应的化学方程式是______.
(6)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件.试根据你的化学知识分析,原因是(用离子方程式表示)______.
解:(1)实验室用A装置制备氯气,经过除杂E装置、干燥F装置后分别通入C、D装置中进行漂白性性质实验,然后通入到B中验证氯气的强氧化性,氯气有毒,不能直接排放到空气中,应用G装置吸收氯气,则各仪器从左至右的连接顺序为A、E、F、C、D、B、G,故答案为:E;F;C;D;B;
(2)浓盐酸有挥发性,所以氯气中含有氯化氢气体,因饱和食盐水中含有大量的Cl-,对Cl2的溶解有抑制作用,使Cl2+H2O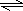 H++Cl-+HClO平衡向左移动,故可用饱和食盐水除去HCl;氯气和水反应生成盐酸和次氯酸,次氯酸具有漂白性,能使有色布条褪色,所以看到的现象是湿润的红色布条褪色;氯气能和碘化钾发生置换反应生成碘单质,所以看到的现象是溶液由无色变为褐色,
H++Cl-+HClO平衡向左移动,故可用饱和食盐水除去HCl;氯气和水反应生成盐酸和次氯酸,次氯酸具有漂白性,能使有色布条褪色,所以看到的现象是湿润的红色布条褪色;氯气能和碘化钾发生置换反应生成碘单质,所以看到的现象是溶液由无色变为褐色,
故答案为:除去氯化氢;湿润的红色布条褪色;溶液由无色变为褐色;
(3)浓盐酸和二氧化锰在加热条件下反应生成氯化锰、氯气和水,离子方程式为:MnO2+4H++2Cl- Mn 2++Cl2↑+2H2O;
Mn 2++Cl2↑+2H2O;
氯气的氧化性大于碘的氧化性,所以氯气能和碘离子发生置换反应生成碘单质,离子方程式为2I-+Cl2=I2+2Cl-;
氯气和氢氧化钠反应生成氯化钠和次氯酸钠、水,离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:MnO2+4H++2Cl- Mn 2++Cl2↑+2H2O;2I-+Cl2=I2+2Cl-;Cl2+2OH-=Cl-+ClO-+H2O;
Mn 2++Cl2↑+2H2O;2I-+Cl2=I2+2Cl-;Cl2+2OH-=Cl-+ClO-+H2O;
(3)MnO2+2HCl(浓)+2HCl(浓)(还原剂) MnCl2+Cl2↑+2H2O 转移电子
MnCl2+Cl2↑+2H2O 转移电子
2mol 1mol 2mol
4mol 2molo 4mol
所以被还原的HCl的物质的量是4mol;生成氯气的物质的量为2mol,
故答案为:4mol;2mol;
(5)一个氯原子得一个电子生成氯离子,一个氯原子失去2个电子生成次氯酸根离子,一个氯原子失去6个电子生成氯酸根离子,且ClO-与ClO3-物质的量之比为1:1,所以得失电子的最小公倍数为8,该反应的化学反应方程式为4Cl2+8NaOH═6NaCl+NaClO3+NaClO+4H2O,
故答案为:4Cl2+8NaOH═6NaCl+NaClO3+NaClO+4H2O;
(6)盐酸有还原性,次氯酸钠在酸性条件下有强氧化性,所以氯离子和次氯酸根离子能发生氧化还原反应生成氯气和水,离子方程式为Cl-+ClO-+2H+═Cl2↑+H2O,
故答案为:Cl-+ClO-+2H+═Cl2↑+H2O.
分析:(1)实验室用A装置制备氯气,经过除杂E装置、干燥F装置后分别通入C、D装置中进行漂白性性质实验,然后通入到B中验证氯气的强氧化性,氯气有毒,不能直接排放到空气中,应用G装置吸收氯气;
(2)饱和食盐水能抑制氯气的溶解,吸收氯化氢;次氯酸能使有色布条褪色;氯气能和碘化钾发生置换反应;
(3)根据离子方程式的书写规则书写,注意单质、弱电解质、氧化物写化学式,可溶性强电解质写离子;
(4)根据转移电子与被氧化的盐酸、氯气之间的关系式计算,注意该反应部分盐酸作还原剂,部分盐酸作酸;
(5)根据得失电子相等写出该反应方程式;
(6)根据氧化还原反应判断生成物,并写出相应的化学反应方程式.
点评:本题考查氯气的制备,题目难度不大,注意氯气的实验室制法以及氯气与次氯酸的性质的不同.
(2)浓盐酸有挥发性,所以氯气中含有氯化氢气体,因饱和食盐水中含有大量的Cl-,对Cl2的溶解有抑制作用,使Cl2+H2O
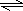 H++Cl-+HClO平衡向左移动,故可用饱和食盐水除去HCl;氯气和水反应生成盐酸和次氯酸,次氯酸具有漂白性,能使有色布条褪色,所以看到的现象是湿润的红色布条褪色;氯气能和碘化钾发生置换反应生成碘单质,所以看到的现象是溶液由无色变为褐色,
H++Cl-+HClO平衡向左移动,故可用饱和食盐水除去HCl;氯气和水反应生成盐酸和次氯酸,次氯酸具有漂白性,能使有色布条褪色,所以看到的现象是湿润的红色布条褪色;氯气能和碘化钾发生置换反应生成碘单质,所以看到的现象是溶液由无色变为褐色,故答案为:除去氯化氢;湿润的红色布条褪色;溶液由无色变为褐色;
(3)浓盐酸和二氧化锰在加热条件下反应生成氯化锰、氯气和水,离子方程式为:MnO2+4H++2Cl-
 Mn 2++Cl2↑+2H2O;
Mn 2++Cl2↑+2H2O;氯气的氧化性大于碘的氧化性,所以氯气能和碘离子发生置换反应生成碘单质,离子方程式为2I-+Cl2=I2+2Cl-;
氯气和氢氧化钠反应生成氯化钠和次氯酸钠、水,离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:MnO2+4H++2Cl-
 Mn 2++Cl2↑+2H2O;2I-+Cl2=I2+2Cl-;Cl2+2OH-=Cl-+ClO-+H2O;
Mn 2++Cl2↑+2H2O;2I-+Cl2=I2+2Cl-;Cl2+2OH-=Cl-+ClO-+H2O;(3)MnO2+2HCl(浓)+2HCl(浓)(还原剂)
 MnCl2+Cl2↑+2H2O 转移电子
MnCl2+Cl2↑+2H2O 转移电子2mol 1mol 2mol
4mol 2molo 4mol
所以被还原的HCl的物质的量是4mol;生成氯气的物质的量为2mol,
故答案为:4mol;2mol;
(5)一个氯原子得一个电子生成氯离子,一个氯原子失去2个电子生成次氯酸根离子,一个氯原子失去6个电子生成氯酸根离子,且ClO-与ClO3-物质的量之比为1:1,所以得失电子的最小公倍数为8,该反应的化学反应方程式为4Cl2+8NaOH═6NaCl+NaClO3+NaClO+4H2O,
故答案为:4Cl2+8NaOH═6NaCl+NaClO3+NaClO+4H2O;
(6)盐酸有还原性,次氯酸钠在酸性条件下有强氧化性,所以氯离子和次氯酸根离子能发生氧化还原反应生成氯气和水,离子方程式为Cl-+ClO-+2H+═Cl2↑+H2O,
故答案为:Cl-+ClO-+2H+═Cl2↑+H2O.
分析:(1)实验室用A装置制备氯气,经过除杂E装置、干燥F装置后分别通入C、D装置中进行漂白性性质实验,然后通入到B中验证氯气的强氧化性,氯气有毒,不能直接排放到空气中,应用G装置吸收氯气;
(2)饱和食盐水能抑制氯气的溶解,吸收氯化氢;次氯酸能使有色布条褪色;氯气能和碘化钾发生置换反应;
(3)根据离子方程式的书写规则书写,注意单质、弱电解质、氧化物写化学式,可溶性强电解质写离子;
(4)根据转移电子与被氧化的盐酸、氯气之间的关系式计算,注意该反应部分盐酸作还原剂,部分盐酸作酸;
(5)根据得失电子相等写出该反应方程式;
(6)根据氧化还原反应判断生成物,并写出相应的化学反应方程式.
点评:本题考查氯气的制备,题目难度不大,注意氯气的实验室制法以及氯气与次氯酸的性质的不同.

练习册系列答案
相关题目

 Cl2↑+MnCl2+2H2O
Cl2↑+MnCl2+2H2O