题目内容
【题目】下列叙述正确的是
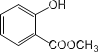
①SO2、CS2、HI都是直线形的分子 ②价电子排布式为ns2的原子属于ⅠA或ⅡA族元素 ③Ge是ⅣA族的一种元素,其核外电子排布式为:[Ar]4s24p2,属于P区元素 ④非极性分子往往是高度对称的分子,比如BF3,PCl5,H2O2,CO2这样的分子⑤化合物NH4Cl和CuSO4·5H2O都存在配位键 ⑥AgCl是一种白色的沉淀,不溶于硝酸、浓硫酸、烧碱溶液,却能溶于氨水中 ⑦已知熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力且可作手术刀的消毒液,则从不同角度分类HgCl2是一种共价化合物、非电解质、盐、分子晶体 ⑧氨水中大部分NH3与H2O以氢键(用“…”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式为![]()
A.①③B.②④C.⑤⑥D.⑤⑦⑧
【答案】C
【解析】
①CS2、HI都是直线形的分子,SO2是“V”形的分子,故①错误;②价电子排布式为ns2的原子属于ⅡA族元素或0族元素,故②错误;③Ge是ⅣA族的一种元素,其核外电子排布式为:[Ar]3d104s24p2,属于p区元素,故③错误;④非极性分子往往是高度对称的分子,比如BF3、PCl5、CO2这样的分子,H2O2是极性分子,故④错误;⑤化合物NH4Cl中铵根存在配位键,CuSO4·5H2O中[Cu(H2O)4]2+存在配位键,故⑤正确;⑥AgCl是一种白色的沉淀,不溶于硝酸、浓硫酸、烧碱溶液,却能溶于氨水中形成[Ag(NH3)2]+,故⑥正确;⑦HgCl2的稀溶液有弱的导电能力说明HgCl2是弱电解质,故⑦错误;⑧氨水中大部分NH3与H2O以氢键(用“···”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式为![]() ,故⑧错误;因此⑤⑥正确,故C正确。
,故⑧错误;因此⑤⑥正确,故C正确。
综上所述,答案为C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案