题目内容
 某校科学兴趣小组探究二氧化碳与过氧化钠反应是否有氧气生成,设计了如图的实验装置.B中盛有饱和碳酸氢钠溶液,吸收挥发出的HCl. E为收集氧气装置.
某校科学兴趣小组探究二氧化碳与过氧化钠反应是否有氧气生成,设计了如图的实验装置.B中盛有饱和碳酸氢钠溶液,吸收挥发出的HCl. E为收集氧气装置.(1)写出装置A中发生反应的化学
(2)C中盛有
(3)写出装置D中发生反应的化学方程式
(4)指出装置E的错误:
考点:钠的重要化合物
专题:几种重要的金属及其化合物
分析:(1)A中用盐酸与碳酸钙反应制取二氧化碳;
(2)从B中出来的气体含有水蒸气,水蒸气能够与过氧化钠反应产生氧气,对检验二氧化碳与过氧化钠反应是否有氧气生成造成干扰;
(3)过氧化钠与二氧化碳反应生成碳酸钠和氧气;
(4)排水法收集氧气,图中导气管气体长进短出,收集不到氧气.
(2)从B中出来的气体含有水蒸气,水蒸气能够与过氧化钠反应产生氧气,对检验二氧化碳与过氧化钠反应是否有氧气生成造成干扰;
(3)过氧化钠与二氧化碳反应生成碳酸钠和氧气;
(4)排水法收集氧气,图中导气管气体长进短出,收集不到氧气.
解答:
解:(1)盐酸与碳酸钙反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)从B中出来的气体含有水蒸气,水蒸气能够与过氧化钠反应产生氧气,对检验二氧化碳与过氧化钠反应是否有氧气生成造成干扰,所以C中可装浓硫酸干燥二氧化碳;
故答案为:浓硫酸;除去二氧化碳中的水蒸气;
(3)过氧化钠与二氧化碳反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2;
故答案为:2Na2O2+2CO2═2Na2CO3+O2;
(4)排水法收集氧气,导气管应短进长出;
故答案为:E中导气管应短进长出.
故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)从B中出来的气体含有水蒸气,水蒸气能够与过氧化钠反应产生氧气,对检验二氧化碳与过氧化钠反应是否有氧气生成造成干扰,所以C中可装浓硫酸干燥二氧化碳;
故答案为:浓硫酸;除去二氧化碳中的水蒸气;
(3)过氧化钠与二氧化碳反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2;
故答案为:2Na2O2+2CO2═2Na2CO3+O2;
(4)排水法收集氧气,导气管应短进长出;
故答案为:E中导气管应短进长出.
点评:本题为实验题,探究二氧化碳与过氧化钠反应是否有氧气生成,熟悉反应的原理和常见仪器的用途是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
分子式C6H12O2的有机物,已知它在NaOH溶液及在稀硫酸中均能发生反应,则符合此条件的该有机物最大有( )
| A、20种 | B、19种 |
| C、17种 | D、15种 |
在2H2SO4(浓)+Cu═CuSO4+SO2↑+2H2O反应中,还原剂与氧化剂物质的量之比为( )
| A、32:49 | B、1:1 |
| C、1:2 | D、2:1 |
在淀粉碘化钾溶液中加入少量NaClO溶液,振荡,溶液变蓝.在上述溶液中加入足量的Na2SO3溶液,蓝色逐渐消失.下列判断错误的是( )
| A、氧化性:ClO->I2 |
| B、蓝色逐渐消失说明Na2SO3具有漂白性 |
| C、漂白粉溶液可使淀粉碘化钾试纸变蓝 |
| D、向新制氯水中加入足量亚硫酸钠溶液,氯水褪色 |
物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关.下列各组物质中由于浓度不同而能发生不同氧化还原反应的是( )
①Cu与HNO3溶液②Fe与HCl溶液③Zn与H2SO4溶液 ④铝与NaOH溶液.
①Cu与HNO3溶液②Fe与HCl溶液③Zn与H2SO4溶液 ④铝与NaOH溶液.
| A、①③ | B、①② | C、②④ | D、②③ |
用NA表示阿伏加德罗常数的值,下列判断正确的是( )
| A、22.4L氢气中含有的氢分子数目是NA |
| B、36gH2O含有的氧原子数目是2NA |
| C、1mol/LBaCl2溶液中含有Cl-数目是2 NA |
| D、1mol H2在Cl2中完全燃烧转移的电子数是NA |
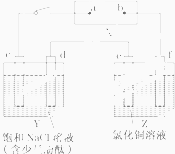 如图X是直流电源.Y槽中c、d为石墨棒,Z槽中e、f是质量相同的铜棒.接通电路后,发现d附近显红色.
如图X是直流电源.Y槽中c、d为石墨棒,Z槽中e、f是质量相同的铜棒.接通电路后,发现d附近显红色.