题目内容
A、W为金属单质,B、X、Y为非金属单质,B与W反应生成棕黄色烟E,D、Z为生活必需物质,相互关系如下图。
请回答:
(1)写出C的化学式:_______________。
(2)写出Y+G![]() W+Z的化学反应方程式,并标明电子转移的方向和数目:____________________________________________________________。
W+Z的化学反应方程式,并标明电子转移的方向和数目:____________________________________________________________。
(3)写出电解D的饱和水溶液的离子方程式:____________________________________。
(4)用电子式表示Z的形成过程:____________。
(1)Na2O
(2)
(3)2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
(4)![]() (写成
(写成![]() 或
或![]() 也可)
也可)
解析:B与W反应生成棕黄色烟E,故B、W、E分别为Cl2、Cu、CuCl2,D是生活必需物质,则D为NaCl,A为Na,X为O2,C为Na2O,H为Na2O2,Z为H2O,J为NaOH。据此即可解答相关问题。

练习册系列答案
相关题目
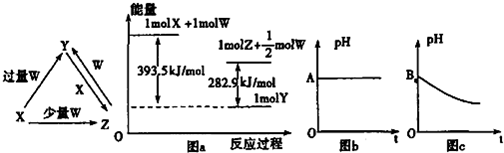
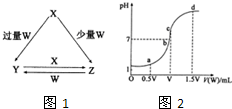 (2013?菏泽二模)X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图1所示(水及部分产物已略去).
(2013?菏泽二模)X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图1所示(水及部分产物已略去). 
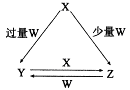
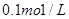 的NaOH溶液滴定
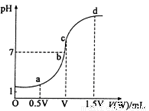
的NaOH溶液滴定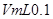 mo1/L HA溶液,滴定曲线如图所示,则a、b、c、d四点溶液中水的电离程度最大的是
点;a点溶液中离子浓度的大小顺序为
;少量c点溶液于试管中,再滴加0.1mo1/L盐酸至中性,此时溶液中除H+、OH-外 ,离子浓度的大小顺序为 。
mo1/L HA溶液,滴定曲线如图所示,则a、b、c、d四点溶液中水的电离程度最大的是
点;a点溶液中离子浓度的大小顺序为
;少量c点溶液于试管中,再滴加0.1mo1/L盐酸至中性,此时溶液中除H+、OH-外 ,离子浓度的大小顺序为 。