题目内容
蓄电池是一种可以反复充电、放电的装置。有一种蓄电池在充电和放电时发生的反应是:NiO2 + Fe + 2H2O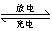 Fe(OH)2 + Ni(OH)2。
Fe(OH)2 + Ni(OH)2。
(1)若此蓄电池放电时,该电池某一电极发生还原反应的物质是 (填序号)。
A.NiO2 B.Fe C.Fe(OH)2 D.Ni(OH)2
(2)用此蓄电池分别电解以下两种溶液,假如电路中转移了0.02 mole-,且电解池的电极均为惰性电极,试回答下列问题。
①电解M(NO3)x溶液时某一电极增加了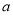 g M,则金属M的相对原子质量为 (用含“
g M,则金属M的相对原子质量为 (用含“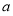 、x”的表达式表示)。
、x”的表达式表示)。
②电解含有0.01 mol CuSO4和0.01 mol NaCl的混合溶液100mL,阳极产生的气体在标准状况下的体积是 ;将电解后的溶液加水稀释至1L,此时溶液的PH= 。
(1)A (2)①50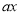 ②0.168; 2
②0.168; 2
【解析】
试题分析:分析蓄电池的反应可知发生还原反应的物质是NiO2,(2)Mx++xe-=M,当增加agM时其相对原子质量为50ax;电解混合溶液时阳极2Cl- -2e-=Cl2↑0.01molCl-失去0.01mole-,而电路中转移0.02mole-,所以溶液中的OH-放电,4OH- -4e-=2H2O+O2↑且失去0.01mole-,生成0.0025mol氧气,所以阳极生成气体的总量为0.0075mol,体积为0.168L.同时溶液中消耗0.01molOH-,H+的物质的量为0.01mol,1L溶液中的c(H+)=0.01mol/L.pH=2.
考点:原电池原理、原电池工作中的计算。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目