��Ŀ����
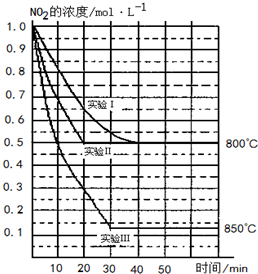
ij�����£���2L�ܱ������з������·�Ӧ2NO2��g��?2NO��g��+O2��g�������ֲ�ͬ�����½��У�����ʵ�����800�棬ʵ�����850�棬NO��O2����ʼŨ�ȶ�Ϊ0��NO2��Ũ����ʱ�䣨min���ı仯��ͼ��ʾ����ش��������⣺
��2L�ܱ������ڣ�800��ʱ��Ӧ��2NO2��g��?2NO��g��+O2��g����ϵ�У�n��NO2����ʱ��ı仯�����
��1��ʵ��������ķ�Ӧ������______
��2��д���÷�Ӧ��ƽ�ⳣ������ʽ��K=______���÷�Ӧ��______��������š����ȷ�Ӧ��
��3����ʵ����д�ƽ��������ܱ�������ͨ��2mol�����ʵ���֮��Ϊ1��1��ɵ�NO2��O2������壨�����¶Ȳ��䣩����ƽ�⽫______�ƶ���
��4�����������ڣ�3�������õ�ƽ��������ͨ��������NaOH��Һ�У�ʹ���屻������գ����ɵIJ��P�����ʵ���Ϊ______��
��5��NO2��NO����Ҫ�Ĵ�����Ⱦ���������������NH3��һ����������֮��Ӧ������ת��Ϊ���IJ������ѭ�������ʣ��÷�Ӧ�Ļ�ѧ����ʽΪ______������дһ����
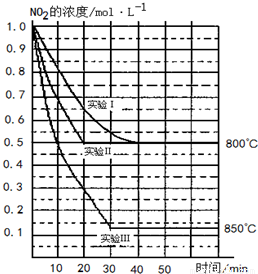
��2����ѧƽ�ⳣ��Ϊ������Ũ����֮���뷴Ӧ��Ũ����֮�ȵıȣ���ͼ��֪���¶�Խ�ߣ�ƽ��ʱNO2��Ũ��ԽС��
��3������ƽ�ⳣ����Ũ�����ж�ƽ���ƶ���
��4������ת��Ϊ��ʼ����֪��NO2�����ʵ���Ϊ1mol/L×2L+1mol=3mol��1molO2����������Һ�з�Ӧ����HNO3������Nԭ���غ������
��5������������ԭ��Ӧ���������Ļ�ѧ��Ӧ��
����⣺��1����ʵ����ʵ���ƽ��ʱNO2��Ũ����ͬ����ʵ���Ӧ���ʴ���ʵ���ʹ���˴������ʴ�Ϊ��ʹ���˴�����
��2���ɷ�Ӧ2NO2��g��?2NO��g��+O2��g������K=
 �����¶�Խ�ߣ�ƽ��ʱNO2��Ũ��ԽС��������ӦΪ���ȷ�Ӧ���ʴ�Ϊ������
�����¶�Խ�ߣ�ƽ��ʱNO2��Ũ��ԽС��������ӦΪ���ȷ�Ӧ���ʴ�Ϊ��������3��ʵ����д�ƽ���c��NO2��=0.5mol/L��
2NO2��g��
 2NO��g��+O2��g��
2NO��g��+O2��g����ʼ��mol/L����1 0 0
�仯��mol/L����0.5 0.5 0.25
ƽ�⣨mol/L����0.5 0.5 0.25
ƽ�ⳣ��k=
 =0.25��
=0.25��ͨ��2mol�����ʵ���֮��Ϊ1��1��ɵ�NO2��O2������壨�����¶Ȳ��䣩��
��ʱΪc��NO2��=0.5mol/L+
 =1mol/L��c��NO��=0.5mol/L��c��O2��=0.25mol/L+
=1mol/L��c��NO��=0.5mol/L��c��O2��=0.25mol/L+ =0.75mol/L��
=0.75mol/L��Ũ����ΪQc=
 =
= =0.1825��0.25��ƽ�������ƶ���
=0.1825��0.25��ƽ�������ƶ����ʴ�Ϊ�����ң�
��4������ת��Ϊ��ʼ����֪��NO2�����ʵ���Ϊ1mol/L×2L+1mol=3mol��1molO2����������Һ�з�Ӧ����HNO3��������NaOH��Ӧ����NaNO3��
��Nԭ���غ��֪��NO2��NaNO3�����Եõ�NaNO3�����ʵ���Ϊ3mol���ʴ�Ϊ��NaNO3��3mol��
��5���������л�ԭ�ԣ�NO2��NO���������ԣ���������ԭ��Ӧת��Ϊ���ĵ������ŷ��ڻ����У�������ԭ��ӦΪ8NH3+6NO2=7N2+12H2O��6NO+4NH3=5N2+6H2O��
�ʴ�Ϊ��8NH3+6NO2=7N2+12H2O��6NO+4NH3=5N2+6H2O��
���������⿼��ͼ���뻯ѧƽ�⣬��ȷӰ�컯ѧƽ������ؼ�ͼ���������ǽ����Ĺؼ�����4����ѧ������е��ѵ㣬ע������K��Q������ƽ���ƶ��ķ�����

��11�֣�ij�����£���2L�ܱ������з������·�Ӧ��2NO2(g)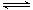 2NO(g)��O2(g) ��H>0�������ֲ�ͬ�����½��У�����NO��O2����ʼŨ�ȶ�Ϊ0 mol/L��ʵ���Ӧ�¶���ͬ��NO2��Ũ��(mol��L��1)��ʱ��(min)�ı仯��ͼ��ʾ����ش��������⣺
2NO(g)��O2(g) ��H>0�������ֲ�ͬ�����½��У�����NO��O2����ʼŨ�ȶ�Ϊ0 mol/L��ʵ���Ӧ�¶���ͬ��NO2��Ũ��(mol��L��1)��ʱ��(min)�ı仯��ͼ��ʾ����ش��������⣺
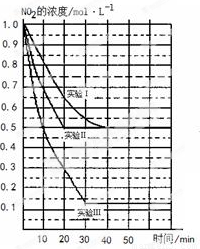
��1������ͼ�б��϶�Ӧ�ķ�Ӧ�¶ȣ�800���850�棩��ʵ��������ķ�Ӧ������_______________________��
��2��д���÷�Ӧ��ƽ�ⳣ������ʽ��K=______________��
|
|
|
 _________��������ƶ����������ƶ������ƶ�����
_________��������ƶ����������ƶ������ƶ�����
��4��һ��������NO2��SO2�ɷ�����Ӧ���䷽��ʽΪ��
NO2(g)��SO2(g)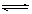 SO3(g)��NO(g) ��H>0����NO2��SO2�������
SO3(g)��NO(g) ��H>0����NO2��SO2������� �����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬���� ���� ��
�����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬���� ���� ��
A����ϵѹǿ���ֲ��� B�����������ɫ���ֲ���
C��SO3��NO������ȱ��ֲ��� D����������ƽ����Է����������ֲ���
��5�����ı�������ʹƽ�ⳣ����÷�Ӧ ���� ��
A��һ��������Ӧ�����ƶ� B����ƽ���ƶ�ʱ������Ӧ������������С
C��һ�����淴Ӧ�����ƶ� D����ƽ���ƶ�ʱ���淴Ӧ������������С
 ij�����£���2L�ܱ������з������·�Ӧ2NO2��g��?2NO��g��+O2��g��
ij�����£���2L�ܱ������з������·�Ӧ2NO2��g��?2NO��g��+O2��g�� 2NO(g)��O2(g) ��H>0�������ֲ�ͬ�����½��У�����NO��O2����ʼŨ�ȶ�Ϊ0 mol/L��ʵ���Ӧ�¶���ͬ��NO2��Ũ��(mol��L��1)��ʱ��(min)�ı仯��ͼ��ʾ��
2NO(g)��O2(g) ��H>0�������ֲ�ͬ�����½��У�����NO��O2����ʼŨ�ȶ�Ϊ0 mol/L��ʵ���Ӧ�¶���ͬ��NO2��Ũ��(mol��L��1)��ʱ��(min)�ı仯��ͼ��ʾ��
 SO3(g)��NO(g) ��H>0����NO2��SO2�������
SO3(g)��NO(g) ��H>0����NO2��SO2������� �����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬���� ���� ��
�����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬���� ���� �� 2NO(g)��O2(g) ��H>0�������ֲ�ͬ�����½��У�����NO��O2����ʼŨ�ȶ�Ϊ0 mol/L��ʵ���Ӧ�¶���ͬ��NO2��Ũ��(mol��L��1)��ʱ��(min)�ı仯��ͼ��ʾ����ش��������⣺
2NO(g)��O2(g) ��H>0�������ֲ�ͬ�����½��У�����NO��O2����ʼŨ�ȶ�Ϊ0 mol/L��ʵ���Ӧ�¶���ͬ��NO2��Ũ��(mol��L��1)��ʱ��(min)�ı仯��ͼ��ʾ����ش��������⣺
 _________��������ƶ����������ƶ������ƶ�����
_________��������ƶ����������ƶ������ƶ����� SO3(g)��NO(g) ��H>0����NO2��SO2�������
SO3(g)��NO(g) ��H>0����NO2��SO2������� �����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬���� ���� ��
�����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬���� ���� �� 2NO(g)��O2(g)
��H>0�������ֲ�ͬ�����½��У�����NO��O2����ʼŨ�ȶ�Ϊ0 mol/L��ʵ���Ӧ�¶���ͬ��NO2��Ũ��(mol��L��1)��ʱ��(min)�ı仯��ͼ��ʾ��
2NO(g)��O2(g)
��H>0�������ֲ�ͬ�����½��У�����NO��O2����ʼŨ�ȶ�Ϊ0 mol/L��ʵ���Ӧ�¶���ͬ��NO2��Ũ��(mol��L��1)��ʱ��(min)�ı仯��ͼ��ʾ��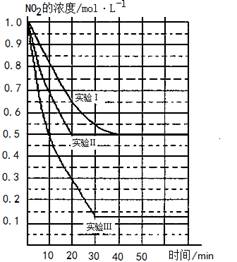
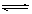 SO3(g)��NO(g) ��H>0����NO2��SO2�������
SO3(g)��NO(g) ��H>0����NO2��SO2�������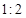 �����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬���� ���� ��
�����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬���� ���� ��