题目内容
下列判断错误的是
A.沸点:NH3>PH3>AsH3
B.结合质子的能力:OH->CH3COO->Cl-
C.酸性:HClO4 >H2SO4 >H3PO4
D.碱性:NaOH >Mg(OH)2 >Al(OH)3
A
【解析】
试题分析:A.结构相似的物质,相等分子质量越大,分子间作用力就越大,物质的熔沸点就越高。由于在NH3的分子之间增加了氢键,使分子之间的吸引力增强,破坏较难,所以沸点最高。故沸点:NH3> AsH3>PH3,错误;B.物质越难电离,则结合质子的能力最强。由于电离程度H2O< CH3COOH<HCl,故结合质子的能力:OH->CH3COO->Cl-,正确;C.元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强。由于元素的非金属性:Cl>S>P,所以酸性:HClO4 >H2SO4 >H3PO4,正确;C.元素的金属性越强,其最高价氧化物对应的水化物的碱性就越强。由于元素的金属性:Na>Mg>Al,所以碱性:NaOH >Mg(OH)2 >Al(OH)3,正确。
考点:考查元素周期律的知识及应用、元素的金属性、非金属性强弱比较的知识。

练习册系列答案
相关题目


 —
—

 ________(填“>”“=”或“<”)
________(填“>”“=”或“<”) 。
。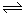 CO2+H2(g)
CO2+H2(g)
