题目内容
下列叙述正确的是
- A.明矾是常用的净水剂,可以杀菌消毒。
- B.分别向澄清石灰水溶液、氯化钙和偏铝酸溶液通入二氧化碳气体过程中都有白色沉淀产生。
- C.CaCO3难溶于水而Ca(HCO3)2易溶于水,可用澄清石灰水鉴别Na2CO3和NaHCO3溶液。
- D.NaOH溶液可区别Na2SO4、MgCl2、FeCl2、Al2(SO4)3四种溶液。
D
正确答案D
A、不正确,明矾在水中Al3++3H2O Al(OH)3+3H+ , Al(OH)具有较强的吸附性,是常用的净水剂,但不可以杀菌消毒。
Al(OH)3+3H+ , Al(OH)具有较强的吸附性,是常用的净水剂,但不可以杀菌消毒。
B、不正确,向氯化钙溶液通入二氧化碳气体没有白色沉淀产生。
C、不正确,CaCO3难溶于水而Ca(HCO3)2易溶于水,不可用澄清石灰水鉴别Na2CO3和NaHCO3溶液,两者与澄清石灰水反应,均产生白色沉淀。
D、NaOH溶液可区别Na2SO4、MgCl2、FeCl2、Al2(SO4)3四种溶液,现象分别是:无明显现象、白色沉淀、灰白色沉淀变成灰绿再变成红褐色、先产生白色沉淀,NaOH过量后沉淀溶解。
正确答案D
A、不正确,明矾在水中Al3++3H2O
 Al(OH)3+3H+ , Al(OH)具有较强的吸附性,是常用的净水剂,但不可以杀菌消毒。
Al(OH)3+3H+ , Al(OH)具有较强的吸附性,是常用的净水剂,但不可以杀菌消毒。B、不正确,向氯化钙溶液通入二氧化碳气体没有白色沉淀产生。
C、不正确,CaCO3难溶于水而Ca(HCO3)2易溶于水,不可用澄清石灰水鉴别Na2CO3和NaHCO3溶液,两者与澄清石灰水反应,均产生白色沉淀。
D、NaOH溶液可区别Na2SO4、MgCl2、FeCl2、Al2(SO4)3四种溶液,现象分别是:无明显现象、白色沉淀、灰白色沉淀变成灰绿再变成红褐色、先产生白色沉淀,NaOH过量后沉淀溶解。

练习册系列答案
相关题目
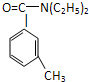 避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH
避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH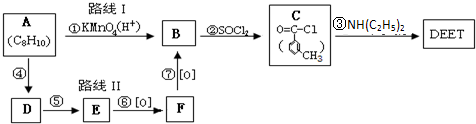
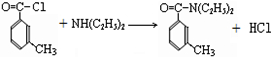
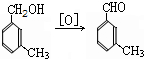
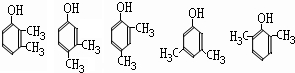 (任写2种)
(任写2种)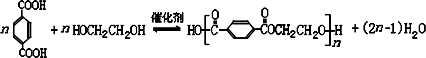
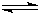 NH3?H2O+H+
NH3?H2O+H+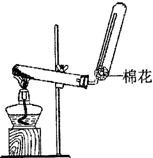 (2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.
(2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.