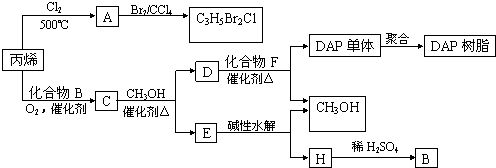
题目内容
(1)HCl的相对分子质量为
(2)0.5mol的Fe含
36.5
36.5
,HCl的摩尔质量为36.5g/mol或36.5g.mol-1
36.5g/mol或36.5g.mol-1
,49g H2SO4的物质的量为0.5mol
0.5mol
;(2)0.5mol的Fe含
0.5NA
0.5NA
个铁原子,质量是28
28
g,12.04×1023个铁原子约是2
2
mol.分析:(1)同一物质的相对分子质量与其摩尔质量在数值上相等,根据n=
计算硫酸的物质的量;
(2)根据N=nNA计算铁原子个数,根据m=nM计算其质量,根据n=
计算物质的量.
| m |
| M |
(2)根据N=nNA计算铁原子个数,根据m=nM计算其质量,根据n=
| N |
| NA |
解答:解:(1)HCl的相对分子质量=1+35.5=36.5,同一物质的相对分子质量与其摩尔质量在数值上相等,所以氯化氢的摩尔质量是36.5g/mol,n( H2SO4)=
=
=0.5mol,
故答案为:36.5;36.5 g/mol或36.5 g.mol-1;0.5mol;
(2)N=nNA=0.5mol×NA/mol=0.5NA,m=nM=0.5mol×56g/mol=28g,n=
=
=2mol,故答案为:0.5NA;28;2.
| m |
| M |
| 49g |
| 98g/mol |
故答案为:36.5;36.5 g/mol或36.5 g.mol-1;0.5mol;
(2)N=nNA=0.5mol×NA/mol=0.5NA,m=nM=0.5mol×56g/mol=28g,n=
| N |
| NA |
| 12.04×1023 |
| 6.02×1023/mol |
点评:本题考查了物质的量的有关计算,掌握基本公式是解本题关键,根据公式分析解答即可,难度不大.

练习册系列答案
相关题目

 )
)
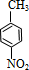
 +HOCH2CH2Cl
+HOCH2CH2Cl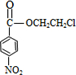 +H2O
+H2O




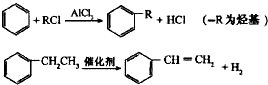
 +CH3CH2Cl
+CH3CH2Cl +HCl
+HCl