题目内容
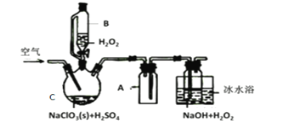
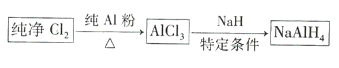
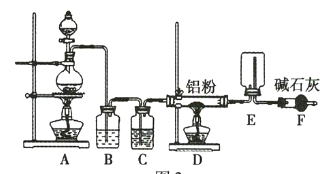
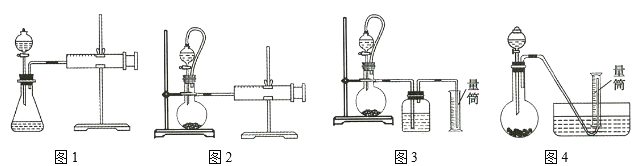
【题目】物质A由三种元素组成。M是单质,空气的主要成分之一。B是一种固体单质,组成该物质的元素在A中的质量分数约为![]() 。C、D均由两种元素组成,C中两元素同主族。I是一种建筑用的黏合剂。各物质之间的转化关系如图:
。C、D均由两种元素组成,C中两元素同主族。I是一种建筑用的黏合剂。各物质之间的转化关系如图:
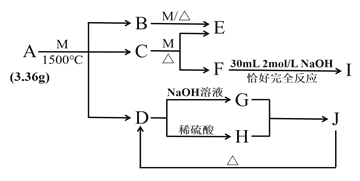
请回答:
![]() 中所含元素是_____________
中所含元素是_____________![]() 填元素名称
填元素名称![]() 。
。
![]() 与M反应的化学方程式为_______________________________________。
与M反应的化学方程式为_______________________________________。
![]() 写出
写出![]() 的离子方程式___________________________________________。
的离子方程式___________________________________________。
![]() 请设计实验方案证明E可能的成分___________________________________________。
请设计实验方案证明E可能的成分___________________________________________。
【答案】铝、硅、碳 ![]()
![]()
![]()
![]() 成分可能是:只有CO;只有
成分可能是:只有CO;只有![]() ;CO和
;CO和![]() 混合物;检验方法:将气体依次通过①澄清石灰水②足量氢氧化钠溶液③澄清石灰水④浓硫酸⑤灼热的氧化铜⑥澄清石灰水⑦燃着的酒精灯或气囊,若只有①变浑浊,则只有
混合物;检验方法:将气体依次通过①澄清石灰水②足量氢氧化钠溶液③澄清石灰水④浓硫酸⑤灼热的氧化铜⑥澄清石灰水⑦燃着的酒精灯或气囊,若只有①变浑浊,则只有![]() ;若①无明显现象,⑤黑色变红色⑥变浑浊,则只有CO;若①变浑浊③无明显现象⑤黑色变红色⑥变浑浊,则E为CO和
;若①无明显现象,⑤黑色变红色⑥变浑浊,则只有CO;若①变浑浊③无明显现象⑤黑色变红色⑥变浑浊,则E为CO和![]() 混合物
混合物
【解析】
C、D均由两种元素组成,由D与酸碱反应知D为氧化铝,G为偏铝酸钠,H为硫酸铝,J为氢氧化铝, M是单质,空气的主要成分之一,是氧气,氮气的化学性质较稳定,排除。F能与30mL,2mol/L氢氧化钠反应,I是一种建筑用的黏合剂,为硅酸钠,F为二氧化硅,C为碳化硅;各种物质的质量可求出A的组成,根据A的性质回答下列问题。E为碳与氧气反应的物质,完全燃烧,不完全燃烧产物不同。
(1)C、D均由两种元素组成,由D与酸碱反应知D为氧化铝,G为偏铝酸钠,H为硫酸铝,J为氢氧化铝, M是单质,空气的主要成分之一,是氧气,氮气的化学性质较稳定,排除。F能与30mL,2mol/L氢氧化钠反应,I是一种建筑用的黏合剂,为硅酸钠,F为二氧化硅,C为碳化硅,根据二氧化硅与氢氧化钠反应的离子方程式可知,![]() ,二氧化硅的物质的量n=
,二氧化硅的物质的量n=![]() =0.03mol,根据硅元素守恒,碳化硅的物质的量也为0.03mol,硅元素的物质的量也为0.03mol,则碳化硅的质量为0.03 mol×40g/mol=1.2g,B是一种固体单质是碳,C中两元素同主族是碳化硅,故A中所含元素是铝、硅、碳 ,B是一种固体单质是碳,组成该物质的元素在A中的质量分数约为
=0.03mol,根据硅元素守恒,碳化硅的物质的量也为0.03mol,硅元素的物质的量也为0.03mol,则碳化硅的质量为0.03 mol×40g/mol=1.2g,B是一种固体单质是碳,C中两元素同主族是碳化硅,故A中所含元素是铝、硅、碳 ,B是一种固体单质是碳,组成该物质的元素在A中的质量分数约为![]() ,A的质量为3.36g,则A中碳元素的质量为3.36g×
,A的质量为3.36g,则A中碳元素的质量为3.36g×![]() =0.9g,碳元素的物质的量为
=0.9g,碳元素的物质的量为![]() =0.075mol,硅元素的质量为0.03 mol×40g/mol×
=0.075mol,硅元素的质量为0.03 mol×40g/mol×![]() =0.84g ,则铝元素的质量为3.36g-0.9g-0.84g=1.62g,n=
=0.84g ,则铝元素的质量为3.36g-0.9g-0.84g=1.62g,n=![]() =0.06mol,故铝,硅,碳元素的物质的量之比等于0.06:0.03:0.075=4:2:5,故A的化学式为
=0.06mol,故铝,硅,碳元素的物质的量之比等于0.06:0.03:0.075=4:2:5,故A的化学式为![]() ,故A中所含元素是铝、硅、碳 ;
,故A中所含元素是铝、硅、碳 ;
(2)![]() 与M反应的化学方程式为:
与M反应的化学方程式为:![]()
![]()
![]() ;
;
(3)![]() 为二氧化硅与氢氧化钠溶液反应,离子方程式为:
为二氧化硅与氢氧化钠溶液反应,离子方程式为:![]() ;
;
(4)成分可能是:只有CO;只有![]() ;CO和
;CO和![]() 混合物。检验方法:将气体依次通过①澄清石灰水②足量氢氧化钠溶液③澄清石灰水④浓硫酸⑤灼热的氧化铜⑥澄清石灰水⑦燃着的酒精灯或气囊,若只有①变浑浊,则只有
混合物。检验方法:将气体依次通过①澄清石灰水②足量氢氧化钠溶液③澄清石灰水④浓硫酸⑤灼热的氧化铜⑥澄清石灰水⑦燃着的酒精灯或气囊,若只有①变浑浊,则只有![]() ;若①无明显现象,⑤黑色变红色⑥变浑浊,则只有CO;若①变浑浊③无明显现象⑤黑色变红色⑥变浑浊,则E为CO和
;若①无明显现象,⑤黑色变红色⑥变浑浊,则只有CO;若①变浑浊③无明显现象⑤黑色变红色⑥变浑浊,则E为CO和![]() 混合物。
混合物。

 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案