题目内容
50mL的酸式滴定管中盛有0.1mol/L的HCl溶液,溶液的凹液面最低点刻度为20.00mL.若将滴定管内的酸液全部放完,刚好中和锥形瓶内30.00mL的NaOH溶液,此碱液的浓度为( )
| A、>0.1mol/L | B、<0.1mol/L | C、=0.1mol/L | D、不能确定 |
分析:滴定管的刻度从上到下,50mL刻度以下还有没有刻度的一部分,若把到20mL刻度位置的液体放出,其液体体积大于(50-20)=30mL,根据物质的量浓度的计算公式求出盐酸的浓度即可.
解答:解:滴定管的刻度从上到下,50mL刻度以下还有没有刻度的一部分,若把到20mL刻度位置的液体放出,其液体体积大于30mL(50mL-20mL),消耗盐酸的体积大于
=0.1mol/L,
故选A.
| 0.1mol/L×0.03L |
| 0.03L |
故选A.
点评:本题考查滴定管的使用,难度不大,注意滴定管的刻度从上到下,最大刻度以下还有没有刻度的一部分.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
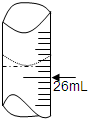 为了测出某氢氧化钠溶液的物质的量浓度,某研究性学习小组先用广泛pH试纸测出该溶液的pH,发现该溶液的pH=14.于是他们用碱式滴定管量取25.00mL待测氢氧化钠溶液盛放在锥形瓶中,把0.1000mol/L的标准盐酸溶液注入50mL的酸式滴定管中,然后进行中和滴定操作.
为了测出某氢氧化钠溶液的物质的量浓度,某研究性学习小组先用广泛pH试纸测出该溶液的pH,发现该溶液的pH=14.于是他们用碱式滴定管量取25.00mL待测氢氧化钠溶液盛放在锥形瓶中,把0.1000mol/L的标准盐酸溶液注入50mL的酸式滴定管中,然后进行中和滴定操作.