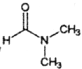
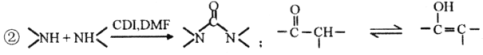��Ŀ����
����Ŀ����.���úϳ�������Ҫ�ɷ�ΪCO��CO2��H2���ڴ����������ºϳɼ״�������������Ӧ���£�
��CO2(g)+3H2(g)![]() CH3OH��g��+H2O(g) ��H1��
CH3OH��g��+H2O(g) ��H1��
��CO(g)+2H2(g)![]() CH3OH(g) ��H2
CH3OH(g) ��H2
��CO2(g)+H2(g)![]() CO(g)+H2O(g) ��H3��
CO(g)+H2O(g) ��H3��
��ѧ�� | H-H | C-O | C | H-O | C-H |
E/��kJ��mol-1�� | 436 | 343 | 1076 | 465 | X |
�ش��������⣺
(1)��֪��H2=-99 kJ��mol-1��������ϱ���صĻ�ѧ�����ܣ���C![]() O����ʾCO�Ļ�ѧ��������X=_______ kJ��mol-1��
O����ʾCO�Ļ�ѧ��������X=_______ kJ��mol-1��
(2)��Ӧ�١��ڡ��۶�Ӧ��ƽ�ⳣ��K1��K2��K3֮��Ĺ�ϵʽΪ___________��
(3)���ݻ�ѧ��Ӧԭ������������ѹǿ�Է�Ӧ�۵�Ӱ��Ϊ_______________������ʾ���ӶԷ�Ӧ���ʡ�ƽ��״̬��ת���ʽǶȻش�
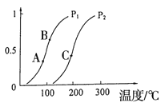
��.�����Դ���й����Ŀ�����Ӧ��ǰ�����ɼ�С��Ⱦ����������⣬���м״������������ʵ����ȼ�ϣ�������ȼ�ϵ�ء�һ����������CO��H2�ϳ�CH3OH��CO��g��+2H2��g��![]() CH3OH��g����H=-99kJmol-1�������Ϊ2L���ܱ������г���2molCO��4molH2����ò�ͬ�¶��������ڵ�ѹǿ��P��kPa����ʱ�䣨min���ı仯��ϵ��ͼ�Т�������ʾ��
CH3OH��g����H=-99kJmol-1�������Ϊ2L���ܱ������г���2molCO��4molH2����ò�ͬ�¶��������ڵ�ѹǿ��P��kPa����ʱ�䣨min���ı仯��ϵ��ͼ�Т�������ʾ��

�٢�͢���ȣ��ı�ķ�Ӧ������_________��
�ڷ�Ӧ����6minʱ�ﵽƽ�⣬�ڴ������´ӷ�Ӧ��ʼ���ﵽƽ��ʱv��CH3OH��=_____��
�۷�Ӧ����2minʱ�ﵽƽ�⣬ƽ�ⳣ��K����=_________��
�ܱȽϷ�Ӧ����¶ȣ�T1���ͷ�Ӧ����¶ȣ�T3���ĸߵͣ�T1_____T3���������������=����
���𰸡�413 K1=K2��K3������K3=K1/K2�� ����ѹǿ����Ӧ���ʼӿ죬ƽ�ⲻ�ƶ�����Ӧ���ת���ʲ��� ʹ�ô��� 0.125 mol/��L��min�� 12 ��
��������
��1���ɢ�CO(g)+2H2(g)![]() CH3OH(g) ��H2=-99 kJ��mol-1������ݱ�����صĻ�ѧ�����ܿ�֪��1076+2��436-3X-343-465=-99�����X=+413��
CH3OH(g) ��H2=-99 kJ��mol-1������ݱ�����صĻ�ѧ�����ܿ�֪��1076+2��436-3X-343-465=-99�����X=+413��
(2)�ɢ�CO2(g)+3H2(g)![]() CH3OH��g��+H2O(g) ��֪��K1=
CH3OH��g��+H2O(g) ��֪��K1=
��CO(g)+2H2(g)![]() CH3OH(g) ��֪��K2=
CH3OH(g) ��֪��K2=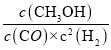
��CO2(g)+H2(g)![]() CO(g)+H2O(g) ��֪��K3==
CO(g)+H2O(g) ��֪��K3==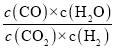
K2![]() K3=
K3= =K1�����Է�Ӧ�١��ڡ��۶�Ӧ��ƽ�ⳣ��K1��K2��K3֮��Ĺ�ϵʽΪK1=K2
=K1�����Է�Ӧ�١��ڡ��۶�Ӧ��ƽ�ⳣ��K1��K2��K3֮��Ĺ�ϵʽΪK1=K2![]() K3��
K3��
(3)���ݷ�Ӧ ��CO2(g)+H2(g)![]() CO(g)+H2O(g) ��H3��֪����Ӧǰ��ѧ��������ȵ����巴Ӧ������ѹǿ��ѧ��Ӧ�������ӣ���ѧƽ�ⲻ�ƶ���ƽ��ת���ʲ��䣻�𰸣�����ѹǿ����Ӧ���ʼӿ죬ƽ�ⲻ�ƶ�����Ӧ���ת���ʲ��䣻
CO(g)+H2O(g) ��H3��֪����Ӧǰ��ѧ��������ȵ����巴Ӧ������ѹǿ��ѧ��Ӧ�������ӣ���ѧƽ�ⲻ�ƶ���ƽ��ת���ʲ��䣻�𰸣�����ѹǿ����Ӧ���ʼӿ죬ƽ�ⲻ�ƶ�����Ӧ���ת���ʲ��䣻
��.����CO(g)+2H2(g)![]() CH3OH(g)��H=-99kJmol-1��ͼ���֪����͢�ﵽƽ��״̬ʱѹǿ��ȣ�����Ȣ��ȴﵽƽ��״̬�����Ըı�ķ�Ӧ����Ӧ��ʹ���˴������𰸣�ʹ�ô�����
CH3OH(g)��H=-99kJmol-1��ͼ���֪����͢�ﵽƽ��״̬ʱѹǿ��ȣ�����Ȣ��ȴﵽƽ��״̬�����Ըı�ķ�Ӧ����Ӧ��ʹ���˴������𰸣�ʹ�ô�����
�ڸ�������ʽ��
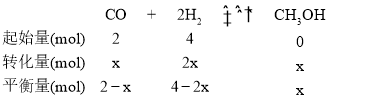
����ͼ����ʼʱѹǿΪΪƽ��ʱѹǿ��2������![]() =
=![]() �����x=15����Ӧ����6minʱ�ﵽƽ��ʱv(CH3OH)=
�����x=15����Ӧ����6minʱ�ﵽƽ��ʱv(CH3OH)=![]() =0.125 mol/(L��min����
=0.125 mol/(L��min����
�۷�Ӧ����2minʱ�ﵽƽ�⣬��������������֪ƽ��ʱc(CH3OH)=![]() =0.75 mol/L��c(CO)=
=0.75 mol/L��c(CO)=![]() =0.25 mol/L��c(H2)=
=0.25 mol/L��c(H2)=![]() =0.5 mol/L����CO(g)+2H2(g)
=0.5 mol/L����CO(g)+2H2(g)![]() CH3OH(g)֪K=
CH3OH(g)֪K=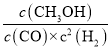 =
=![]() =12���𰸣�12��
=12���𰸣�12��
����CO(g)+2H2(g)![]() CH3OH(g)��ͼ���֪���ﵽƽ�����ѹǿС�ڢ�˵��ƽ�������ƶ�����Ϊ�Ƿ��ȷ�Ӧ������T1��T3��
CH3OH(g)��ͼ���֪���ﵽƽ�����ѹǿС�ڢ�˵��ƽ�������ƶ�����Ϊ�Ƿ��ȷ�Ӧ������T1��T3��

����Ŀ��Cl2��һ����Ҫ�Ļ���ԭ�ϣ�Ҳ��һ�־綾���塣ij��ѧ��ȤС���Ʊ�Cl2��̽��Cl2������ʵĹ������¡��ش��������⣺
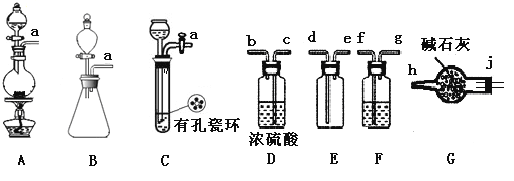
(1)�������Ʊ�
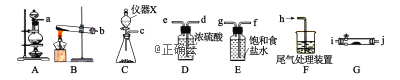
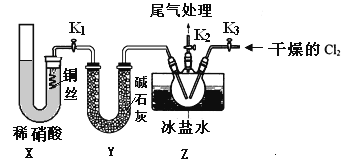
����ͼ������X��������_________________������KMnO4��ŨHCl��Ӧ�Ʊ�Cl2������Ӧ�Ļ�ѧ����ʽΪ_______________________________________________________��
�����ö������̺�Ũ�����Ʊ����������Cl2�������ӿڵ�����˳��Ϊ_______________������������������Сд��ĸ˳����д����
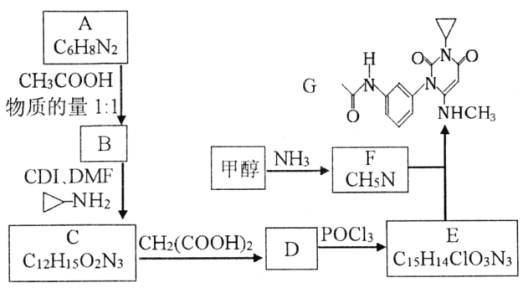
(2)�Ʊ���������Fe����Ӳ�ʲ�����G�еķ�Ӧ�����ȡ________��Ӧ����������Ӧ���Ӳ�ʲ������й�������ϡ���ᣬȡ�����ܽ�����Һ��������н������������ࣺ
ʵ���� | ʵ����� | ʵ������ | ʵ����� |
�� | ȡ��������Һ���μ�______��Һ | ____________ | ����Fe2+ |
�� | ȡ��������Һ���μ�______��Һ | ____________ | ����Fe3+ |