题目内容
14.下列有机含氧酸,其酸性强弱顺序正确的是( )| A. | 硫酸>磷酸>高氯酸 | B. | 硫酸>高氯酸>磷酸 | ||
| C. | 高氯酸>硫酸>磷酸 | D. | 高氯酸>磷酸>硫酸 |
分析 同周期自左而右非金属性增强,非金属性越强,最高价含氧酸的酸性越强.
解答 解:同周期自左而右非金属性增强,非金属性Cl>S>P,非金属性越强,最高价含氧酸的酸性越强,故酸性高氯酸>硫酸>磷酸,故C正确;
故选C.
点评 本题考查元素周期表与周期律的递变性,明确同周期、同主族元素的性质变化规律及元素非金属性的比较方法是解答本题的关键,难度不大.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
5.下列有关氧化还原反应的叙述正确的是( )
| A. | 元素化合价升高的反应是还原反应 | |
| B. | 物质在变化中失去了电子,此物质中的某一元素化合价降低 | |
| C. | 有电子转移的反应就是氧化还原反应 | |
| D. | 有化合价升降的反应,不一定是氧化还原反应 |
2.下列有关元素的性质及递变规律中错误的是( )
| A. | IA族与VIIA族元素间可形成共价化合物或离子化合物 | |
| B. | 第三周期元素从左到右,最高正价从+1 递增到+7 | |
| C. | 同主族元素的简单阴离子还原性越强,其在水中越容易水解 | |
| D. | 同周期的主族金属元素的化合价越高,其原子失电子能力越弱 |
9.某药物中间体的合成路线如图所示.下列说法正确的是( )


| A. | 对苯二酚在空气中能稳定存在 | |
| B. | 1mol该中间体最多可与11mol H2反应 | |
| C. | 2,5羟基苯乙酮能发生加成、氧化、还原、缩聚反应 | |
| D. | 该中间体分子中含有1个手性碳原子 |
19.下列叙述中,能肯定A金属比B金属活泼性强的是( )
| A. | A原子的最外层电子数比B原子的最外层电子数少 | |
| B. | A原子的电子层数比B原子的电子层数多 | |
| C. | 1 molA从酸中置换出的H2比1 molB从酸中置换出的氢气多 | |
| D. | 常温时,A能从水中置换出氢气而B不能 |
6.下表是A、B、C、D、E五种有机物的有关信息:
回答下列问题:
(1)A~E中,属于烃的是AB(填字母).A中含官能团名称是碳碳双键.
(2)A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br.
(3)C催化氧化生成D的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(4)有机物B具有的性质是②③(填序号).
①无色无味的液体;②有毒;③不溶于水;④密度比水大;⑤能使酸性KMnO4溶液和溴水褪色.
| A | ①能使溴的四氯化碳溶液褪色; ②比例模型为  ③能与水在一定条件下反应生成C |
| B | ①由C、H两种元素组成;②球棍模型为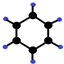 |
| C | ①由C、H、O三种元素组成;②能与Na反应; ③与E反应生成相对分子质量为88的酯 |
| D | ①相对分子质量比C少2;②能由C催化氧化得到 |
| E | ①由C、H、O三种元素组成;②其水溶液能使紫色石蕊试液变红 |
(1)A~E中,属于烃的是AB(填字母).A中含官能团名称是碳碳双键.
(2)A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br.
(3)C催化氧化生成D的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(4)有机物B具有的性质是②③(填序号).
①无色无味的液体;②有毒;③不溶于水;④密度比水大;⑤能使酸性KMnO4溶液和溴水褪色.

 A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H溶液中的溶质是一种盐.它们的转化关系如图所示.请回答:
A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H溶液中的溶质是一种盐.它们的转化关系如图所示.请回答: ;
; ;
; .
.