��Ŀ����
���淴ӦA(g)+3B(g) 2C(g) ��H����QkJ/mol���мס��������ݻ���ͬ�Ҳ�����ܱ���������������м���1 mol A��3 mol B����һ�������´ﵽƽ��ʱ�ų�����ΪQ1kJ������ͬ�������£����������м���2 mol C�ﵽƽ�����������ΪQ2
kJ����֪Q1��3Q2��������������ȷ����
2C(g) ��H����QkJ/mol���мס��������ݻ���ͬ�Ҳ�����ܱ���������������м���1 mol A��3 mol B����һ�������´ﵽƽ��ʱ�ų�����ΪQ1kJ������ͬ�������£����������м���2 mol C�ﵽƽ�����������ΪQ2
kJ����֪Q1��3Q2��������������ȷ����
A������A��ת����Ϊ75�� B��Q1+Q2��Q
C���ﵽƽ����������м���0.25 mol A��0.75 mol B��1.5 mol C��ƽ���������ƶ�
D�����е��Ȼ�ѧ����ʽΪ2C��g�� A��g��+3B��g�� ��H����Q2 kJ/mol
A��g��+3B��g�� ��H����Q2 kJ/mol
D
��������
�����������Q1��3Q2��֪��n����A����3��n����A������
��
A��g��+3B��g��  2C��g��
2C��g��
��ʼ����mol�� 1 3 0
ת������mol�� x 3x 2x
ƽ������mol�� 1-x 3-3x 2x
�� A��g��+3B��g��  2C��g��
2C��g��
��ʼ����mol�� 0 0 2
ת������mol��  x
x 
ƽ������mol��  x 2��
x 2��
���á�һ�ߵ���������֪��1
mol A��3 mol B���롰2 mol C���ǵ�Ч���ϣ�������ͬ��ͬ�ݵ������½�����ƽ��״̬��ȫ��ͬ����1��x�� �����x��0.75�����Ԧ�(A)��
�����x��0.75�����Ԧ�(A)�� ��100%��75%�����A��ȷ��B��Q1+Q2��0.75Q+
��100%��75%�����A��ȷ��B��Q1+Q2��0.75Q+ Q��Q ������B��ȷ��C�����á�һ�ߵ���������֪�ټ��롰0.25 mol A��0.75 mol B��1.5 mol C�����ټ��롰2 mol C����Ч���ں��º����������൱������ѹǿ��ƽ��������C�ķ����ƶ�����C��ȷ��D�����з�Ӧ����CΪ
Q��Q ������B��ȷ��C�����á�һ�ߵ���������֪�ټ��롰0.25 mol A��0.75 mol B��1.5 mol C�����ټ��롰2 mol C����Ч���ں��º����������൱������ѹǿ��ƽ��������C�ķ����ƶ�����C��ȷ��D�����з�Ӧ����CΪ mol��0.50mol�������Ȼ�ѧ����ʽ��2 mol C��Ӧ�ķ�Ӧ��ӦΪ��4Q2 kJ•mol-1����D����ѡD��
mol��0.50mol�������Ȼ�ѧ����ʽ��2 mol C��Ӧ�ķ�Ӧ��ӦΪ��4Q2 kJ•mol-1����D����ѡD��
���㣺�����Чƽ���Ӧ�á���Ӧ�ȵļ����Լ����淴Ӧ���йؼ����

��һ�������£������ܱ������н��еĿ��淴ӦA(g)��3B(g)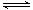
|
A��A��B��C�ķ�����֮��Ϊ1��3��2
B��A��B��C��Ũ�����
C����λʱ������ n mol A��ͬʱ���� 3n mol B
D������C��������C�ֽ���������
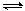
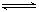 2C(g)�ﵽƽ��״̬�ı�־��
2C(g)�ﵽƽ��״̬�ı�־�� nC(g)
(����Ӧ����)������C��Ũ����ѹǿ�仯������ƽ��Ĺ�ϵͼ,��nֵ��ѹǿP1��P2�Ĺ�ϵ��ȷ����
nC(g)
(����Ӧ����)������C��Ũ����ѹǿ�仯������ƽ��Ĺ�ϵͼ,��nֵ��ѹǿP1��P2�Ĺ�ϵ��ȷ����