题目内容
14.能与SO2气体发生反应,但无沉淀产生的是( )①氯水 ②Ba(OH)2溶液 ③石灰水 ④Na2CO3溶液 ⑤稀硫酸 ⑥Na2SO3溶液.
| A. | 只有① | B. | ①③④ | C. | ④⑤⑥ | D. | ①④⑥ |
分析 二氧化硫具有强还原性能与强氧化性的物质反应,二氧化硫为酸性氧化物,与碱、盐溶液以及氧化性物质等发生反应,结合强酸制取弱酸的反应原理来解答.
解答 解:①氯水与二氧化硫反应生成盐酸和硫酸,没有生成沉淀,故正确;
②Ba(OH)2溶液与二氧化硫反应生成亚硫酸钡沉淀,故错误;
③石灰水与二氧化硫反应生成亚硫酸钙沉淀,故错误;
④Na2CO3与二氧化硫反应生成亚硫酸钠和二氧化碳气体,没有生成沉淀,故正确;
⑤稀H2SO4与二氧化硫不反应,故错误;
⑥Na2SO3与二氧化硫反应生成亚硫酸氢钠,没有生成沉淀,故正确.
故选D.
点评 本题考查了物质性质的应用,为高频考点,侧重于学生的分析能力的考查,注意二氧化硫化学性质的分析判断,题目较简单.

练习册系列答案
相关题目
5.含有CO、N2、H2、CO2和少量水蒸气的混合气体,依次通过足量的灼热氧化铜、浓氢氧化钠溶液、浓硫酸后,剩余的气体是( )
| A. | N2 | B. | N2和H2 | C. | N2和CO2 | D. | H2和CO |
2.2000年前的《神农本草经》就有麻黄能“治咳逆上气”额记载,它的结构简式为 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 麻黄的分子式为C10 H17O | |
| B. | 麻黄可以从植物中提取 | |
| C. | 麻黄在空气中燃烧有NO释出 | |
| D. | 麻黄的一溴代物有3种且可与HCl反应 |
9.能证明SO2是酸性氧化物的是( )
| A. | 酸性KMnO4溶液中通入SO2气体后紫红色消失 | |
| B. | 滴有酚酞的NaOH溶液中通入SO2气体后红色消失 | |
| C. | 品红溶液中通入SO2气体后红色消失 | |
| D. | 溴水中通入SO2气体后橙色消失 |
19.下列不是离子化合物的是( )
| A. | HCl | B. | CaI2 | C. | KOH | D. | NaNO3 |
6.设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A. | 1 mol甲基(-CH3)所含电子数为9NA | |
| B. | 26 g C2H2和苯蒸气的混合气体中所含的C原子数为2NA | |
| C. | 标准状况下,B2H6(g)和C2H4的混合气体22.4 L,所含的电子数约为16NA | |
| D. | 在浓硫酸作用下,60g冰醋酸与足量无水乙醇反应生成乙酸乙酯的分子数为NA |
3.实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH $→_{170℃}^{浓硫酸}$CH2=CH2,CH2=CH2+Br2→BrCH2CH2Br.用少量的溴和足量的乙醇制备l,2-二溴乙烷的装置如右图所示,有关数据如表:
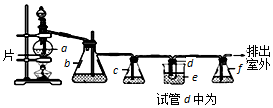
回答下列问题:
(1)在装置c中应加入③(选填序号),其目的是吸收反应中可能生成的酸性气体.
①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)将二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的下层.(填“上”或“下”)
(3)判断d管中制备二溴乙烷反应已结束的最简单方法是溴的颜色完全褪去.
(4)若产物中有少量未反应的Br2,最好用②(填正确选项前的序号)洗涤除去.
①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)以1,2-二溴乙烷为原料,制备聚氯乙烯,为了提高原料利用率,有同学设计了如下流程:1,2-二溴乙烷通过(①)反应制得(②),②通过(③)反应制得氯乙烯,由氯乙烯制得聚氯乙烯.
①消去反应(填反应类型),其化学方程式 .
.
②加成反应(填反应类型).

| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)在装置c中应加入③(选填序号),其目的是吸收反应中可能生成的酸性气体.
①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)将二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的下层.(填“上”或“下”)
(3)判断d管中制备二溴乙烷反应已结束的最简单方法是溴的颜色完全褪去.
(4)若产物中有少量未反应的Br2,最好用②(填正确选项前的序号)洗涤除去.
①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)以1,2-二溴乙烷为原料,制备聚氯乙烯,为了提高原料利用率,有同学设计了如下流程:1,2-二溴乙烷通过(①)反应制得(②),②通过(③)反应制得氯乙烯,由氯乙烯制得聚氯乙烯.
①消去反应(填反应类型),其化学方程式
 .
.②加成反应(填反应类型).
10.下列说法正确的是( )
| A. | 铅蓄电池工作时,电解质溶液H2SO4的浓度不变 | |
| B. | 加水稀释0.1 mol•L-1CH3COOH溶液时,CH3COOH的电离程度增大,pH减小 | |
| C. | 在同浓度的盐酸中,ZnS可溶而CuS不溶,说明CuS的溶解度比ZnS的小 | |
| D. | 标准状况下,2.24 LCCl4含有的共价键数为0.4×6.02×1023个 |