题目内容
已知:① 2CO(g)+O2(g)===2CO2(g) ΔH=-568kJ/mol
② H2(g)+1/2O2(g)=H2O(g) ΔH=―248kJ·mol-1
已知CO和H2的混合物1mol在氧气中充分燃烧放出的热量272KJ,则该混合气体中CO和氢气的物质的量的比值为
A.1:1 B.3:37 C.2:1 D.3:2
【答案】
C
【解析】根据十字交叉法可知,混合气体中CO和氢气的物质的量的比值为 ,答案选C。
,答案选C。

练习册系列答案
相关题目
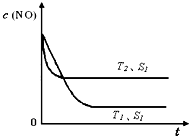 (2012?佛山二模)2012年2月27日深圳宣称进入“200万辆汽车时代”,汽车尾气已成为重要的空气污染物.
(2012?佛山二模)2012年2月27日深圳宣称进入“200万辆汽车时代”,汽车尾气已成为重要的空气污染物. CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95×1011
CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95×1011 CH3CH2OH(g)+H2O(g) 25℃时,K=1.71×1022
CH3CH2OH(g)+H2O(g) 25℃时,K=1.71×1022