题目内容
【题目】下列说法正确的是
A.硼的电负性和硅相近
B.π键是由两个p轨道“肩并肩”重叠形成的,呈轴对称。
C.Cl2是双原子分子,H2S是三原子分子,这是由共价键的方向性决定的
D.原子和其它原子形成共价键时,其共价键数一定等于原子的价电子数
【答案】A
【解析】
A.B、Si在元素周期表中位于对角线位置,性质相似,其电负性相近,故A正确;
B.π键是由两个p轨道“肩并肩”重叠形成的,为镜面对称,故B错误;
C.Cl2是双原子分子,H2S是三原子分子,这是由共价键的饱和性决定的,故C错误;
D.例如P元素形成PCl3时共价键数不等于原子的价电子数,故D错误;
故答案为A。

【题目】利用化学反应原理回答下列问题:
(1)在一定条件下,将1.00molN2(g)与3.00molH2(g)混合于一个10.0L密闭容器中,在不同温度下达到平衡时NH3(g)的平衡浓度如图所示.其中温度为T1时平衡混合气体中氨气的体积分数为25.0%.

①该反应的焓变△H__0.(填“>”或“<”)
②该反应在T1温度下5.00min达到平衡,这段时间内N2的化学反应速率为______.
③T1温度下该反应的化学平衡常数K1=______.
(2)科学家采用质子高导电性的SCY陶瓷(可传递H+)实现了低温常压下高转化率的电化学合成氨,其实验原理示意图如图所示,则阴极的电极反应式是____________.

(3)已知某些弱电解质在水中的电离平衡常数(25℃)如表:
弱电解质 | H2CO3 | NH3H2O |
电离平衡常数 | Ka1=4.30×10﹣7 Ka2=5.61×10﹣11 | Kb=1.77×10﹣5 |
现有常温下0.1molL﹣1的(NH4)2CO3溶液,
①该溶液呈__性(填“酸”、“中”、“碱”),原因是___________.
②该(NH4)2CO3溶液中各微粒浓度之间的关系式不正确的是__.
A.c(NH4+)>c(CO32﹣)>c(HCO3﹣)>c(NH3H2O)
B.c(NH4+)+c(H+)=c(HCO3﹣)+c(OH﹣)+c(CO32﹣)
C.c(CO32﹣)+c(HCO3﹣)+c(H2CO3)=0.1mol/L
D.c(NH4+)+c(NH3H2O)=2c(CO32﹣)+2c(HCO3﹣)+2c(H2CO3)
E.c(H+)+c(HCO3﹣)+c(H2CO3)=c(OH﹣)+c(NH3H2O)
【题目】回答下列以下有关酶的问题:
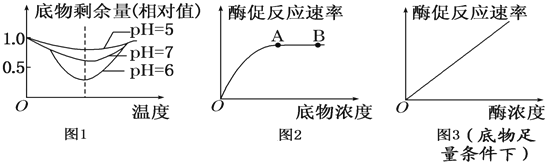
(1)由图1曲线可知:当pH从5上升到7,酶活性的变化过程是 ;从图示曲线还可以得出的结论是 .
(2)图2和图3是底物浓度和酶浓度对酶促反应的影响曲线,请分析回答:
图2中A点后酶促反应的速率不再增加,其限制性因素主要是 .从图3可以得出的结论是:在底物足量的条件下, .
(3)以下是一个有关酶的实验,根据表格内容分析回答下列问题:
操作步骤 | 操作方法 | 试管A | 试管B | 试管C |
1 | 加淀粉溶液 | 2mL | 2mL | 2mL |
2 | 加淀粉酶溶液 | 1mL | 1mL | 1mL |
3 | 温度处理 | 60℃ | 100℃ | 0℃ |
4 | 加碘液 | 2滴 | 2滴 | 2滴 |
①表中为探究 的实验.
②请指出实验操作步骤存在的问题 .
③该实验把温度处理改为pH分别为5、7、9能否用于探究pH对酶活性的影响? 说明理由 .


