题目内容
11.下列有关实验操作和现象、结论都正确的是( )| 选项 | 实验操作和现象 | 实验结论 |
| A | 常温下,将大小、形状形态的锌和铝分别加入到等体积98%的浓硫酸中,观察到前者反应速率快 | 锌比铝活泼 |
| B | 向某溶液中加入盐酸酸化的氯化钡溶液,产生白色沉淀 | 该溶液中一定含有SO42- |
| C | 将盐酸滴入碳酸钠溶液中,产生气泡 | 非金属性:Cl大于C |
| D | 向某溶液中加入氢氧化钡溶液丙加热,产生的气体能使湿润的红色石蕊试纸变蓝 | 该溶液中一定含有NH4+ |
| A. | A | B. | B | C. | C | D. | D |
分析 A.铝与浓硫酸发生钝化现象,无法比较二者金属性强弱;
B.原溶液中可能含有银离子,不一定含有硫酸根离子;
C.盐酸不是最高价含氧酸,无法据此比较Cl、C的非金属性;
D.产生的气体能使湿润的红色石蕊试纸变蓝,该气体为氨气,说明原溶液中含有铵根离子.
解答 解:A.Al在浓硫酸中发生钝化,阻止了反应的继续进行,无法判断二者金属性强弱,故A错误;
B.向某溶液中加入盐酸酸化的氯化钡溶液,产生白色沉淀,该沉淀可能为AgCl,原溶液中含有含有银离子,不一定含有SO42-,故B错误;
C.HCl不是最高价含氧酸,不能根据HCl与碳酸的酸性强弱判断Cl、C的非金属性强弱,故C错误;
D.向某溶液中加入氢氧化钡溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,该气体一定我氨气,则该溶液中一定含有NH4+,故D正确;
故选D.
点评 本题考查化学实验方案的评价,题目难度不大,涉及金属性、非金属性强弱比较及离子检验等知识,明确常见离子的性质及检验方法为解答关键,注意掌握比较金属性、非金属性的方法,试题培养了学生的化学实验能力.

练习册系列答案
相关题目
1.不同温度下BaCO3在水中的沉淀溶解平衡曲线如图所示(已知T1<T2<T3),下列说法正确的是( )
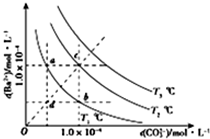

| A. | T2温度下将d点的溶液蒸发浓缩可变为c点 | |
| B. | a点的Ksp小于B点的Ksp | |
| C. | b点溶液中加入BaCl2固体可变为c点 | |
| D. | a点溶液蒸发浓缩恢复到原温度可变为b点 |
2.下列叙述正确的是( )
| A. | 元素的单质一定由氧化或还原该元素的化合物制得 | |
| B. | 一个氧化还原反应中,氧化剂和还原剂一定是两种不同的物质 | |
| C. | 阳离子只能得到电子被还原,阴离子只能失去电子被氧化 | |
| D. | 含有最高价元素的化合物不一定具有很强的氧化性 |
19.下列说法中,正确的是( )
| A. | SO2能使酸性KMnO4溶液褪色,说明SO2具有还原性 | |
| B. | SO2能使品红溶液褪色,其漂白原理与氯水相同 | |
| C. | SO2是酸性氧化物,可以用澄清石灰水来鉴别SO2与CO2 | |
| D. | 用水吸收硫在过量氧气中燃烧的产物,可用于工业制备硫酸 |
6. 如图所示,夹子开始处于关闭状态,将液体A96℃的水①空气(标准大气压)气体B②液体A夹子滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B组合
如图所示,夹子开始处于关闭状态,将液体A96℃的水①空气(标准大气压)气体B②液体A夹子滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B组合
不可能是下列的( )
 如图所示,夹子开始处于关闭状态,将液体A96℃的水①空气(标准大气压)气体B②液体A夹子滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B组合
如图所示,夹子开始处于关闭状态,将液体A96℃的水①空气(标准大气压)气体B②液体A夹子滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B组合不可能是下列的( )
| A. | NaOH溶液、CO2 | B. | H2O、NH3 | C. | NaOH溶液、NO | D. | H2O、NO2 |
16. 某化学兴趣小组设置了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质,下列说法不正确的是( )
某化学兴趣小组设置了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质,下列说法不正确的是( )
 某化学兴趣小组设置了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质,下列说法不正确的是( )
某化学兴趣小组设置了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质,下列说法不正确的是( )| A. | 利用I、II装置制取气体(K2关闭、K1打开),可以在II中收集H2等气体,但不能收集HCl气体 | |
| B. | 若装置II中装满水后,可以收集O2、NO等气体,但不能收集NO2、CO2等气体 | |
| C. | 利用I、Ⅲ装置(K1关闭、K2打开,A中装硝酸)可以比较N、C、Si元素非金属性强弱 | |
| D. | 若在Ⅲ装置的小试管C中加入一定量CCl4和AgNO3溶液(导管伸入CCl4层),则利用I、Ⅲ装置(K1关闭、K2打开)可验证苯与液溴发生的是取代反应,不是加成反应 |
3.18克葡萄糖(C6H12O6)与32克氧气充分反应生成二氧化碳和水蒸气,将生成的气体缓缓通过足量的过氧化钠固体,则固体增重( )克.
| A. | 18 | B. | 16 | C. | 32 | D. | 不能确定 |
 的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
 到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是____________________。
到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是____________________。

 /L的溶液中可能大量存在K+、I-、Mg2+、NO3-
/L的溶液中可能大量存在K+、I-、Mg2+、NO3-