题目内容
|
化学反应可视为旧键断裂和新键形成的过程,共价键的键能是两种原子间形成 1 mol共价键(或其逆过程)时释放(或吸收)的能量.已知H-H键的键能为436 kJ/mol,Cl-Cl键的键能为243 kJ/mol,H-Cl键的键能为431 kJ/mol,那么2HCl(g)=H2(g)+Cl2(g)的ΔH等于 | |
| [ ] | |
A. |
- 183 kJ/mol |
B. |
+ 183 kJ/mol |
C. |
- 862 kJ/mol |
D. |
+ 862 kJ/mol |
答案:B
解析:
解析:
|
本题根据反应热等于反应物键能之和减去生成物键能之和.即Δ H=2×431 kJ/mol-436 kJ/mol-243 kJ/mol=183 kJ/mol. |

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
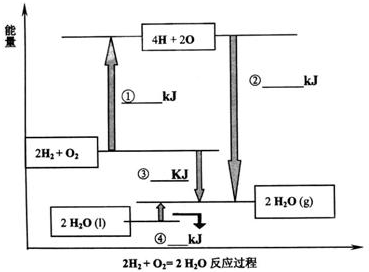
 (1)在25℃、101kPa状况下,4g氢气和适量氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式:
(1)在25℃、101kPa状况下,4g氢气和适量氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式: (2011?宝鸡模拟)化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷(P4)和P4O6的分子结构如图所示;
(2011?宝鸡模拟)化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷(P4)和P4O6的分子结构如图所示; 化学反应可视为旧键断裂和新键形成的过程.已知断开1mol下列化学键时需要吸收的能量分别为:P-P 198kJ、P-O 360kJ、O=O 498kJ
化学反应可视为旧键断裂和新键形成的过程.已知断开1mol下列化学键时需要吸收的能量分别为:P-P 198kJ、P-O 360kJ、O=O 498kJ