题目内容
已知:2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ/mol
Na2O2(s)+CO2(g)===Na2CO3(s)+O2(g) ΔH=-452 kJ/mol
根据以上热化学方程式判断,下列说法正确的是
A.CO的燃烧热为283 kJ
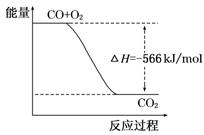
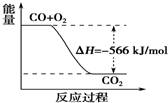
B.下图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)===2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.021023
【答案】
C
【解析】燃烧热单位是kJ/mol,A不正确。B不正确,应该是2molCO和1mol氧气反应生成2molCO2的能量变化图。气态CO2的能量高于固态CO2的能量,所以气态CO2和过氧化钠反应发出的热量多,但放热越多,△H越小,C正确。根据盖斯定律可知,(①+②)÷2即得到Na2O2(s)+CO(g)===Na2CO3(s),所以反应热是(-566 kJ/mol-452kJ/mol)÷2=-509 kJ/mol,在反应中转移电子是2mol,D不正确。答案选C。

练习册系列答案
相关题目