题目内容
【题目】磷单质及其化合物有广泛应用。
(1)三聚磷酸可视为三个磷酸分子之间脱去两个水分子的产物,三聚磷酸钠(俗称“磷酸五钠”)是常用的水处理剂,其化学式为___________________。
(2)次磷酸钠(NaH2PO2)可用于化学镀镍。
①NaH2PO2中P元素的化合价为____________。
②化学镀镍的溶液中含有Ni2+和H2PO![]() ,在酸性条件下发生下述反应,请配平:
,在酸性条件下发生下述反应,请配平:
Ni2++_______H2PO![]() +_______
+_______![]() =_______Ni++_______H2PO
=_______Ni++_______H2PO![]() +_______
+_______![]()
(3)磷酸钙与焦炭、石英砂混合,在电炉中加热到1 500 ℃生成白磷,反应为
2Ca3(PO4)2+6SiO2![]() 6CaSiO3+P4O10
6CaSiO3+P4O10
10C+P4O10![]() P4+10CO
P4+10CO
若反应生成31 g P4,则反应过程中转移的电子数为____________(用NA表示阿伏加德罗常数的值)。
【答案】(1)Na5P3O10
(2)①+1 ②2 1 1 H2O 2 1 2 H+(3)5NA
【解析】
试题分析:(1)相邻的磷酸分子中1个去掉羟基,一个去掉氢原子即可形成三聚磷酸,结构简式为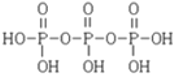 ;三聚磷酸与5分子氢氧化钠反应生成三聚磷酸钠化学式为:Na5P3O10;故答案为:Na5P3O10;
;三聚磷酸与5分子氢氧化钠反应生成三聚磷酸钠化学式为:Na5P3O10;故答案为:Na5P3O10;
(2)由氧化还原反应中化合价升降相等进行配平:镍元素的化合价降低了2价,磷元素的化合价升高的2价,所以根据原子守恒结合电荷守恒可得配平的方程式为:H2O+Ni2++H2PO2-═Ni+H2PO3-+2H+,镍离子被还原成金属Ni,还原产物为Ni,故答案为:1;1;H2O;1;1;2H+;
(3)P由+5价变成0价,每生成1 mol P4时,转移电子20 mol。31 g P4的物质的量为0.25 mol,所以反应转移的电子数为5NA,故答案为:5NA。