题目内容
 燃烧法是测定有机化合物化学式的一种重要方法.取0.1mol某烃完全燃烧,燃烧产物依次通过如图所示的装置,实验结束后,称得甲装置增重5.4g,乙装置增重26.4g
燃烧法是测定有机化合物化学式的一种重要方法.取0.1mol某烃完全燃烧,燃烧产物依次通过如图所示的装置,实验结束后,称得甲装置增重5.4g,乙装置增重26.4g(1)求该烃的分子式
(2)该烃不能因化学反应使溴水和酸性KMnO4溶液褪色,写出其二氯代物可能的结构简式.
考点:有机物实验式和分子式的确定
专题:烃及其衍生物的燃烧规律
分析:(1)甲装置增重为水的质量,乙装置增重为二氧化碳的质量,根据质量可计算C、H原子的物质的量,进而求得该有机物的分子式;
(2)根据性质确定该烃为苯,二氯代物有邻间对三种.
(2)根据性质确定该烃为苯,二氯代物有邻间对三种.
解答:
解:(1)甲装置增重为水的质量,乙装置增重为二氧化碳的质量,
则n(H2O)=
=0.3mol,n(H)=0.6mol,
则1mol烃中含有6molH原子,
n(CO2)=
=0.6mol,n(C)=0.6mol,
则1mol烃中含有6molC原子,
所以该烃的分子式为C6H10,
答:该烃的化学式为C6H6;
(2)该烃不能因化学反应使溴水和酸性KMnO4溶液褪色,故为苯,二氯代物为邻间对三种,结构简式为

 ,
,
答:结构简式为

 .
.
则n(H2O)=
| 5.4g |
| 18g/mol |
则1mol烃中含有6molH原子,
n(CO2)=
| 26.4g |
| 44g/mol |
则1mol烃中含有6molC原子,
所以该烃的分子式为C6H10,
答:该烃的化学式为C6H6;
(2)该烃不能因化学反应使溴水和酸性KMnO4溶液褪色,故为苯,二氯代物为邻间对三种,结构简式为


 ,
,答:结构简式为


 .
.
点评:本题考查有机物分子式的确定,题目难度不大,注意计算分子式的角度,注意结构简式的书写.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案
相关题目
如图为阿司匹林(用T代表)的结构,下列说法不正确的是( )


| A、T可以发生酯化反应 |
| B、T可以与NaOH溶液反应 |
| C、T属于芳香烃类化合物 |
| D、T在酸中水解可以得到CH3COOH |
下列有关物质结构的表述正确的是( )
A、次氯酸的电子式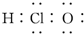 ? ? |
| B、二氧化硅的分子式SiO2 |
C、硫原子结构示意图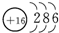 |
D、钠离子的结构示意图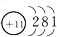 |
把70%的硝酸溶液(ρ=1.40g/cm3)加到等体积的水中,则稀释后硝酸溶液中溶质的质量分数为( )
| A、等于35% | B、小于35% |
| C、大于35% | D、无法确定 |
取一块金属钠放在燃烧匙里加热,观察到下列实验现象:①金属先熔化;②在空气中燃烧,放出紫色火花;③燃烧后生成白色固体;④燃烧时火焰呈黄色;⑤燃烧后生成淡黄色固体物质.其中描述正确的是( )
| A、①② | B、①②③ |
| C、④⑤ | D、①④⑤ |
下列有关实验操作的说法中,不正确的是( )
| A、振荡试管中的液体时,应用手指拿住试管,左右摆动手腕振荡试管 |
| B、在做蒸馏实验时要加入少量的碎瓷片,以防止溶液暴沸 |
| C、如果皮肤上不慎沾上浓硫酸,应立即用大量的NaOH稀溶液冲洗 |
| D、用石蕊或酚酞试纸进行气体验满时,最好先用蒸馏水湿润 |
反应N2+3H2?2NH3△H=-92KJ/mol,决定该反应速率大小的最主要因素是( )
| A、温度 |
| B、N2、H2的性质 |
| C、压强 |
| D、催化剂 |