题目内容
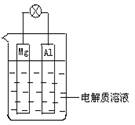
如图所示,组成一种原电池.试回答下列问题(灯泡功率合适):

(1)电解质溶液为稀H2SO4时,灯泡________(填“亮”或“不亮”).若灯泡亮,则Mg电极上发生的反应为________;Al电极上发生的反应为:________.若灯泡不亮,其理由为:________.
(2)电解质溶液为NaOH(aq)时,灯泡________(填“亮”或“不亮”).若灯泡亮,则Mg电极上发生的反应为:________;Al电极上开始时发生的反应为:________.若灯泡不亮,其理由为:________
答案:
解析:
解析:
|
答案:(1)亮 Mg→Mg2++2e- 2H++2e-→H2↑ 硫酸太稀,没有足够的阴、阳离子 (2)亮 6H++6e-→3H2↑ 2Al→2Al3++6e- Al3++4OH- 电解质中没有足够的阴、阳离子 思路解析:(1)、(2)两种情况都具备了形成原电池的条件,因而灯泡都亮.当电解质为酸溶液时,Mg比Al活泼,Mg作原电池的负极,失去电子变为Mg2+;Al作原电池的正极,电子由镁片流向铝片.正极上H+得电子变为H2. 当电解质为碱溶液时,Al与碱反应: 2Al+2NaOH+6H2O 而Mg与碱不反应.所以Al作原电池的负极,负极上Al失去电子流向正极;Mg作正极,正极上H+得电子变成H2. |

练习册系列答案
相关题目
 如图所示,组成一种原电池.试回答下列问题(灯泡功率合适):
如图所示,组成一种原电池.试回答下列问题(灯泡功率合适):