题目内容
日常生活中使用的铝合金中的铝来自于电解氧化铝.工业上电解氧化铝要求其纯度不得低于98.2%,而天然铝土矿的氧化铝含量为50%~70%,杂质主要为SiO2、Fe2O3、CaO、MgO、Na2O等.工业生产铝锭的工艺流程示意图如下: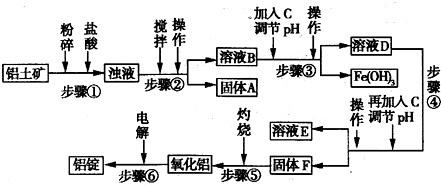
一些氢氧化物沉淀的pH如表:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 |
| 开始沉淀pH(离子初始浓度为0.01mol/L) | 4 | 2.3 | 10.4 |
| 完全沉淀pH(离子初始浓度为<10-5mol/L) | 5.2 | 4.1 | 12.4 |
请回答下列问题:
(1)实验室进行步骤④的操作名称为______.
(2)固体A的化学式为______,物质C的化学式为______.
(3)步骤④调节pH的范围为______.
(4)步骤⑥反应的化学方程式为______.
故答案为:过滤;
(2)由工艺流程可知,步骤①加入盐酸,Si02不与盐酸反应,过滤得到的固体A为SiO2;
由工艺流程可知,溶液B中含有Fe3+,加入C调节pH值后,通过过滤得到沉淀Fe(OH)3,故加入C调节pH值的目的是将Fe3+转化为Fe(OH)3,除去Fe3+,溶液B中含有Na+、Ca2+、Mg2+,故C最好选择NaOH 或Ca(OH)2溶液,
故答案为:SiO2;NaOH 或Ca(OH)2;
(3)步骤④中调节溶液pH,使铝离子沉淀完全而Mg2+离子不产生沉淀,由表中数据可知,pH=4时铝离子开始沉淀,pH=5.2时铝离子完全沉淀,Mg2+开始沉淀溶液的pH=10.4,所以要使铝离子沉淀完全而Mg2+离子不产生沉淀,则步骤④调节pH的范围为:5.2<pH<10.4,
故答案为:5.2<pH<10.4;
(4)工业上采用电解氧化铝的方法冶炼铝,反应方程式为:2Al2O3(熔融)
 4Al+3O2↑,
4Al+3O2↑,故答案为:2Al2O3(熔融)
 4Al+3O2↑.
4Al+3O2↑.分析:(1)由工艺流程可知,步骤④调节pH值后,将固体与液体分离,应采用过滤的方法;
(2)由工艺流程可知,步骤①加入盐酸,SiO2不与盐酸反应,过滤得到的固体A为SiO2;
由工艺流程可知,溶液B中含有Fe3+,加入C调节pH值后,通过过滤得到沉淀Fe(OH)3,故加入C调节pH值的目的是将Fe3+转化为Fe(OH)3,除去Fe3+,结合溶液B中含有的阳离子判断;
(3)步骤④中调节溶液pH,使铝离子沉淀完全而Mg2+离子不产生沉淀,结合离子开始沉淀与沉淀完全的pH解答;
(4)工业上采用电解熔融氧化铝的方法冶炼铝.
点评:本题考查元素化合物性质、化学工艺流程等,理解工艺流程是解题的关键,需要学生根据工艺流程提取信息,对学生综合运用能力和推理有较高的要求,难度中等.

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案金属铝广泛应用于现代生产和日常生活中。
已知:4Al(s)+3O2(g)=2Al2O3(s) △H=-3351.4 kJ?mol-1
4Fe(s)+3O2(g)=2Fe2O3(s) △H=-1633.2 kJ?mol-1
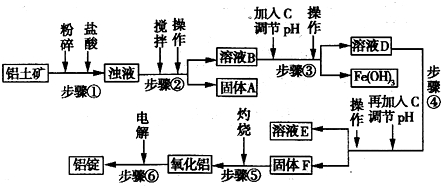
![]() △H=-5518 kJ?mol-1
△H=-5518 kJ?mol-1
将铝用作燃料已成为现实。回答下列问题:
(1)写出工业制铝的阳极电极反应式 。
(2)①铝用作燃料相对于含碳燃料有明显优点,请你写出其中一条 ;
②铝用作燃料相对于氢气也有明显优点,但也有不足,即燃点高。若要在常温常压不使用催化剂的情况下点燃铝,除了应防止表面生成致密的氧化膜外,还应采取的措施是 。
(3)铝热反应在生产中的应用非常广泛。请写出Fe2O3(s)和Al(s)反应的热化学方程式 ;
铝热实验中能看到有熔融物生成,为探究该熔融物的成分,某学生查阅资料如下:
| 物质 | A1 | A12O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | ― |
经分析,该同学推测,铝热反应所得到的熔融物应是铁铝合金。请设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝(简述实验操作、现象及结论) 。
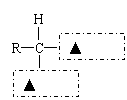 ③蛋白质在人体内水解的最终产物是氨基酸。请在下图虚线方框内写上适当的官能团符号,将氨基酸的通式补充完整:
③蛋白质在人体内水解的最终产物是氨基酸。请在下图虚线方框内写上适当的官能团符号,将氨基酸的通式补充完整: