题目内容
用Na2CO3·10H2O晶体,配制0.2 mol·L-1的Na2CO3溶液480 mL。
(1)应称取Na2CO3·10H2O晶体的质量为 。
(2)根据下列操作对所配溶液的浓度产生的影响,完成下列要求:
①Na2CO3·10H2O晶体失去了部分结晶水
②碳酸钠晶体不纯,其中混有氯化钠
③称量碳酸钠晶体时所用砝码生锈
④容量瓶未经干燥使用
其中引起所配溶液浓度偏高的有 (填序号,下同),偏低的有 ,无影响的有 。
(3)某同学改用固体Na2CO3配制上述Na2CO3溶液的过程如图所示:
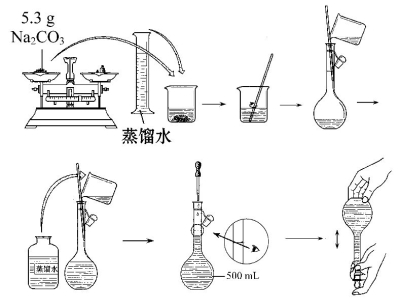
你认为该同学的错误步骤有 (填序号)。
A.1处 B.2处 C.3处 D.4处
(1)28.6 g (2)①③ ② ④ (3)B
【解析】
试题分析:(1)配制0.2 mol·L-1的Na2CO3溶液480 mL实际上应该配制500 mL溶液,故需要Na2CO3·10H2O 0.1 mol,质量为28.6 g。
(2)Na2CO3·10H2O晶体失去了部分结晶水会使得称量的固体中Na2CO3的物质的量比理论值大,会引起所配溶液的浓度偏高;碳酸钠晶体不纯,其中混有氯化钠会使得称量的固体中Na2CO3的物质的量比理论值小,会引起所配溶液的浓度偏低;称量碳酸钠晶体时所用砝码生锈会使得称量的晶体的质量增大,使溶液的浓度偏高;容量瓶未经干燥就使用对溶液的浓度没有影响。
(3)称量的固体的质量错误,应该是10.6 g;定容时不应该仰视。
考点:溶液的配制及分析

练习册系列答案
 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目

 的总物质的量为0.9 mol
的总物质的量为0.9 mol