题目内容
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH.
②有关有机物的沸点见下表:
|
试剂 |
乙醚 |
乙醇 |
乙酸 |
乙酸乙酯 |
|
沸点(℃) |
34.5 |
78.3 |
118 |
77.1 |
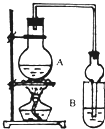
某课外活动小组设计的实验室制取较多量乙酸乙酯的装置如图所示,A中放有乙醇、无水醋酸和浓硫酸,B中放有饱和碳酸钠溶液.试回答:
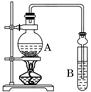
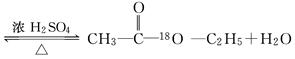
(1)A中浓硫酸的作用是________;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:______________________.
(2)B中球形管的两个作用是________、________.若反应前向B中溶液滴加几滴酚酞,呈红色,产生此现象的原因是__________________________(用离子方程式表示);反应结束后B中的现象是______________________________.
(1)催化剂、吸水剂
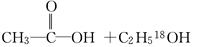
(2)冷凝蒸气 防止倒吸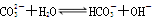 溶液分层,上层无色油状液体,下层溶液颜色变浅
溶液分层,上层无色油状液体,下层溶液颜色变浅
【解析】
试题分析:(1)酯化反应是可逆反应,所以在酯化反应中,浓硫酸起催化剂和吸水剂的作用。酯化反应中羧酸提供羟基,醇提供氢原子,所以反应的化学方程式是
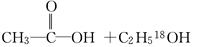
 。
。
(2)由于乙酸和乙醇都是易挥发的,所以生成的乙酸乙酯中混有乙酸和乙醇。又因为二者和水都是互溶的,所以B中球形管的两个作用是冷凝蒸气 防止倒吸;碳酸钠是强碱弱酸盐,水解呈碱性,因此反应前向B中溶液滴加几滴酚酞,呈红色。乙酸乙酯不溶于饱和碳酸钠溶液,密度比水小,有香味,在上层。乙酸和碳酸钠反应而使溶液红色变浅,即下层溶液颜色变浅。
考点:考查乙酸乙酯制备实验的有关判断
点评:该题是中等难度的试题,试题基础性强,难易适中,侧重对学生基础知识的巩固与训练,有利于培养学生的创新思维能力,以及规范、严谨的实验设计与操作能力。该题主要是从乙酸乙酯制取实验的原理、操作、装置、现象上进行分析,以实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案 乙酸乙酯的实验室和工业制法常采用如下反应:
乙酸乙酯的实验室和工业制法常采用如下反应:CH3COOH+C2H5OH
| ||
| △ |
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2?6C2H5OH;
②部分有机物的沸点:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点(℃) | 34.5 | 78.5 | 117.9 | 77 |
(1)浓硫酸的作用是
(2)用如图所示装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为
(3)实验所得到的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,除去
(4)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂,且能重复使用.实验数据如下表所示(乙酸和乙醇以等物质的量混合).
| 同一反应时间 | 同一反应应温度 | ||||
| 反应温度/℃ | 转化率(%) | 选择性(%)* | 反应时间/h | 转化率(%) | 选择性(%)* |
| 40 | 77.8 | 100 | 2 | 80.2 | 100 |
| 60 | 92.3 | 100 | 3 | 87.8 | 100 |
| 80 | 92.6 | 100 | 4 | 92.3 | 100 |
| 120 | 94.5 | 98.7 | 6 | 93.0 | 100 |
| *选择性100%表示反应生成的产物全部是乙酸乙酯和水 | |||||
a.120℃,4hb.80℃,2hc.60℃,4hd.40℃,3h
②当反应温度达到120℃时,反应选抒性降低的原因可能为
 I.下列实验设计、操作或实验现象合理的是
I.下列实验设计、操作或实验现象合理的是A.将纤维素和硫酸混合共热后的液体,取出少许,加入新制的Cu(OH)2悬浊液加热,观察是否有砖红色沉淀生成,以证明纤维素水解生成葡萄糖
B.液态溴乙烷中加入稀NaOH溶液共煮几分钟,然后加入足量稀HNO3,再加入AgNO3溶液检验Br-的生成
C.检验甲酸中是否混有甲醛,可向样品中加入足量NaOH溶液以中和HCOOH,再做银镜反应实验
D.分离苯和苯酚的混合液,加入适量浓溴水,过滤,即可分离
E.将铜丝在酒精灯外焰上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色
F.提取溶解在水中的少量碘:加入酒精,振荡、静置分层后,取出有机层再分离
G.在试管中加入2mL10%的CuSO4溶液,滴入2%的NaOH溶液4~6滴,振荡后加入乙醛溶液0.5mL,加热至沸腾,证明乙醛的性质
Ⅱ.已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2?6C2H5OH.
②有关有机物的沸点:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点(℃) | 34.7 | 78.5 | 118 | 77.1 |
(1)A中浓硫酸的作用是
(2)若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学反应方程式
(3)该实验中使用球形管除起冷凝作用外,另一重要作用是
(4)反应结束后D中的现象是
(5)从B中分离出的乙酸乙酯中还含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,过滤分离出
A 五氧化二磷 B 碱石灰 C 无水硫酸钠 D 生石灰.
 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2?6C2H5OH
②有关有机物的沸点:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/ | 34 | 78.5 | 118 | 77 |
(1)浓硫酸的作用是
(2)球形干燥管C的作用是
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出
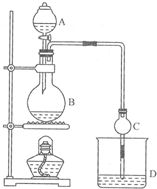 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液. 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.