题目内容
某温度T下,在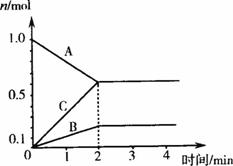
图2-6
(1)由图中的数据分析,该反应的化学方程式为______________________。反应开始至2min,C的平均反应速率为__________________。
(2)如果该反应的逆反应是用于工业上制某种物质的,写出该反应的逆反应·所选择的反应温度:___________,压强:___________。
(3)已知B+C![]() A中AH<0,现分别把2molB和6molC在相同温度和相同容积下,通入甲、乙两容器中,如图2-7所示,甲、乙均为易传热容器,乙是气球,请回答:
A中AH<0,现分别把2molB和6molC在相同温度和相同容积下,通入甲、乙两容器中,如图2-7所示,甲、乙均为易传热容器,乙是气球,请回答:

图2-7
①当反应达到平衡后,两容器内压强P甲__________________P乙。两容器内SO3的物质的量n甲_________n乙(填“>”或“<”或“=”)。
②达到平衡后打开K,乙(气球)的体积将如何变化?_________理由是:____________________
_____________________________________________________________________。
(1)![]() B +
B +
(2)
(3)①< < ②体积减少 理由见下面解析
提示:(1)写反应的化学方程式关键要确定A、B、C之间谁是反应物,谁是生成物,以及方程式中A、B、C三种物质的化学计量数。确定反应物和生成物,主要是看反应过程中各物质的有关量的变化情况。一般反应物物质的量随反应的进行不断减小,生成物的物质的量随反应的进行不断增加,化学计量数之比等于相应物质的物质的量变化之比,结合图示即可求出该反应逆反应B+![]()
![]() 2NH3,该反应的条件为①温度
2NH3,该反应的条件为①温度![]()

 氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义.
氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义.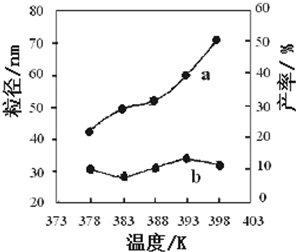 I.高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
I.高炉炼铁是冶炼铁的主要方法,发生的主要反应为: