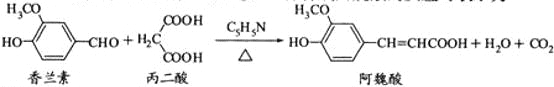题目内容
【题目】酯类化合物与格氏试剂(RMgX,X=Cl、Br、I)的反应是合成叔醇类化合物的重要方法,可用于制备含氧多官能团化合物。化合物F合成路线如下,回答下列问题:
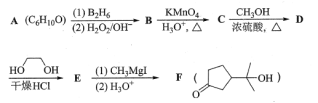
已知信息如下:
①RCH=CH2![]() RCH2CH2OH
RCH2CH2OH
②![]()
③RCOOCH3![]()
(1)A的结构简式为___,B→C的反应类型为__,C中官能团的名称为__,C→D的反应方程式为___。
(2)写出符合下列条件的D的同分异构体__(填结构简式,不考虑立体异构)。
①含有五元碳环结构;②能与NaHCO3溶液反应放出CO2;③能发生银镜反应。
(3)判断化合物F中有无手性碳原子,若有用“*”标出。__
(4)已知羟基能与格氏试剂发生反应。写出以![]() 、CH3OH和格氏试剂为原料制备
、CH3OH和格氏试剂为原料制备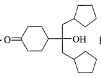 的合成路线(其它试剂任选)。__
的合成路线(其它试剂任选)。__
【答案】 氧化反应 羰基和羧基
氧化反应 羰基和羧基 
 、
、 、
、![]()


【解析】

⑴根据题中信息得出A的结构简式为 ,
, 的过程为氧化过程;C中含有双官能团分别为羰基和羧基;C→D的过程发生的是酯化反应,方程式为
的过程为氧化过程;C中含有双官能团分别为羰基和羧基;C→D的过程发生的是酯化反应,方程式为 ,故答案为:
,故答案为: ;氧化反应;羰基和羧基;
;氧化反应;羰基和羧基; 。
。
⑵根据题目中要求,D( )的同分异构体中需含有五元环、羧基和醛基,因此结构为
)的同分异构体中需含有五元环、羧基和醛基,因此结构为 、
、 、
、 ,故答案为:
,故答案为: 、
、 、
、 。
。
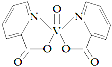
⑶化合物F中含有手性碳原子, ,故答案为:
,故答案为: 。
。
⑷依据所给信息,可得出目标产物的合成路线为: ,故答案为:
,故答案为: 。
。

【题目】Mn、Fe均为第4周期过渡金属元素,两元素的部分电离能数据如下表:
元素 | Mn | Fe | |
电离能/(kJ·mol-1) | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
回答下列问题:
(1)Mn元素基态原子价电子层的电子排布式为__;比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是__。
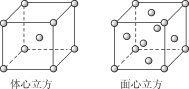
(2)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为__,Fe原子配位数之比为__。